
下列说法正确的是( )
A.硫单质常存在于火山喷口附近
B.进行SO2性质探究实验时,多余的SO2应排到实验室外
C.SO2气体通入BaCl2溶液中不能产生白色沉淀
D.硫在空气中的燃烧产物是SO2,在纯氧中的燃烧产物是SO3
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
绿色化学对化学反应提出了“原子经济性” 的新概念及要求。理想的原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放。下列几种生产乙苯的方法中,原子经济性最好的是(反应均在一定条件下进行) ( )
A.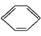 +C2H5Cl
+C2H5Cl
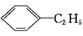 +HCl B.
+HCl B. +C2H5OH
+C2H5OH
 +H2O
+H2O
C. +CH2
+CH2 CH2
CH2

D.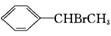

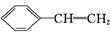 +HBr
+HBr
 +H2
+H2

查看答案和解析>>
科目:高中化学 来源: 题型:
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
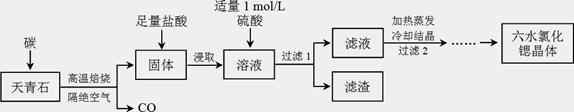
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是_________________________________________。
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_____________________________________________。
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_______________。
(4)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(5)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
① 滴定反应达到终点的现象是_________________________________________。
② 若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
向BaCl2溶液中通入SO2至饱和,此过程无明显实验现象。再向溶液中加入一种物质,溶液变浑浊。加入的这种物质不可能是( )
A.FeCl3溶液 B.NH4Cl溶液 C.稀氨水 D.AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
(1)C的原子结构示意图为__________________
(2)A与G形成的化合物X的结构式为____________,其中X中含有的化学键是______ __,
X属于_________化合物(填“离子”或“共价”)。
(3)比较非金属性强弱G _____ H(填“>”或“<”)。
(4)在一定条件下,A与E可形成一种化合物Y,其相对分子质量与O2相同,则Y为___ ___; Y可在纯氧中燃烧,所得产物无污染,涉及的化学方程式为___________ ______
(5)“神舟”六号载人飞船内需要用化合物Z(由上表中的某2种元素组成)来吸收航天员呼出的CO2,请用化学方程式表示吸收原理___________ ________
(6)E的气态氢化物与其最高价氧化物水化物反应的产物W在一定温度下分解,生成两种氧化物,每1 mol W分解时转移的电子为4 mol ,W受热分解的化学方程式为__ __
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学用如图所示的装置来探究SO2的性质。
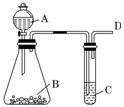
(1)实验前首先应做的操作是_________________________________________________。
(2)实验室用亚硫酸钠固体与较浓硫酸反应制取SO2气体,写出该反应的化学方程式:________________________________________________________________________。
(3)分别将SO2气体通入下列C溶液中,请回答下列问题:
 ①若C为紫色石蕊试液:
①若C为紫色石蕊试液:
| 操作 | 现象 |
| 通入少量SO2 | |
| 继续通入过量SO2 |
②若C为品红溶液:
| 操作 | 现象 |
| 通入足量SO2 | |
| 将试管加热 |
③若C为酸性KMnO4溶液,通入足量SO2,现象______________,KMnO4被________。
④若C为澄清石灰水,通入足量SO2,现象__________________,发生反应的离子方程式________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
A.X使蔗糖变黑的现象主要体 现了X的强氧化性
现了X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可以观察到白色沉淀产生
D.工业上,B转化为D的反应条件为高温、常压、使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B两种烃,其含碳的质量分数相同。关于A和B的叙述中,正确的是( )
A.烃A和B的实验式相同
B.烃A和B一定是同分异构体
C.烃A和B不可能是同系物
D.烃A和B各取1 mol,完全燃烧时消耗氧气的质量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别有10 mL相同浓度的盐酸,将两个 侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
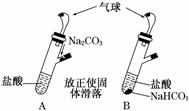
A.A装置的气球膨胀速率大
B.若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L
D.最终两试管中Na+、Cl-的物质的量一定相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com