

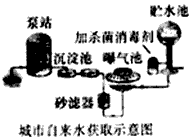
①格栅间,除去污水中的大块物体。
②曝气沉砂池,使砂、水初步分离。
③初次沉淀池,使泥、水分离。
④曝气池,通过微生物的代谢作用,将污水中各种复杂的有机污染物降解为简单的、无害的物质。
⑤二次沉淀池,将水进一步沉淀除杂。
⑥一级处理采用的是物理方法,除去水中的不溶物,包括格栅间、曝气沉砂池和初次沉淀池三个部分。一级处理实际上是对污水的预处理,还没有达到排放标准。
⑦二级处理采用的是生物方法及某些化学方法来除去水中的可降解有机物和部分胶体污染物,包括曝气池和二次沉淀池两个部分。二级处理后的水可达到农田灌溉及排放标准。
⑧三级处理是最终的处理程序,采用的是化学沉淀法、氧化还原法、离子交换法和反渗透法等,是对污水进行深度处理和净化。经三级处理后的水可作为回用水用于绿化和景观用水等。


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
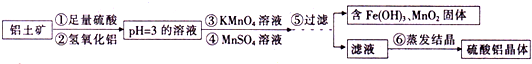
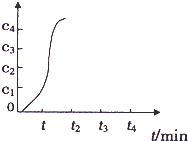
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
I. A~J分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:
(1)A、B、C、D、E、F六种物质中含有的同一种元素在周期表中位置 ,
(2)写出反应④的离子方程式 。
(3)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的
pH 7 (填“>”、“<”或“=”),用离子方程式表示其原因: 。
II.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
(1)电解池阳极的电极反应分别是
① ; ②。
(2)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是 。
(3)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况) L。
查看答案和解析>>
科目:高中化学 来源:期末题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com