
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
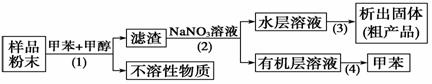
下列说法错误的是 ( )
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚
D.步骤(4)需要蒸馏装置
科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
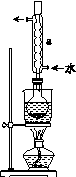
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O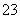 +I2===S4O
+I2===S4O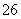 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
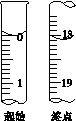
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO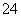 ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )
A. 溴水、氯化铁溶液 B. 溴水、酸性高锰酸钾溶液
C. 溴水、碳酸钠溶液 D. 氯化铁溶液、酸性高锰酸钾溶
查看答案和解析>>
科目:高中化学 来源: 题型:
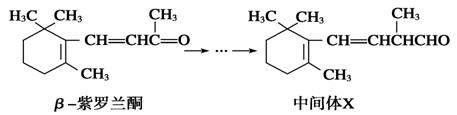
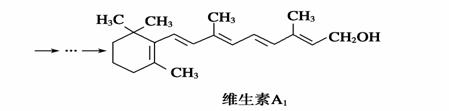
β紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。
下列说法正确的是 ( )
A.维生素A1易溶于NaOH溶液
B.1 mol中间体X最多能与2 mol H2发生加成反应
C.β紫罗兰酮可使酸性KMnO4溶液褪色
D.β紫罗兰酮与中间体X互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有( )。
A.15种 B.28种 C.32种 D.40种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应属于加成反应的是
A.油脂的皂化反应 B.苯与浓硝酸、浓硫酸混合反应
C.在一定条件下,苯与氢气的反应 D.乙烯通入溴的四氯化碳溶液中的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
A、元素的化学性质随着相对原子质量的递增而呈周期性变化
B、元素周期律的实质是因为元素原子最外层电子数由1→8周期性变化而引起的
C、半径由大到小、氧化性由弱到强的是:K+、Mg2+、Al3+、H+,而还原性由弱到强的则是:I-、Br-、Cl-、F-
D、某元素R的最高价氧化物化学式为:R2O5,又知R的气态氢化物中含氢的质量分数为8.8%,则R的相对原子质量为28
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com