
【题目】空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.
(1)上述3种气体直接排入空气后会引起酸雨的气体有(填化学式).
(2)处理酸雨市场采用NaClO2溶液作为吸收剂,可同时对烟气进行脱硫、脱硝,其中脱硫反应ClO2﹣+2SO32﹣2SO42﹣+Cl﹣ , 该反应的平衡常数K的表达式为;
(3)利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,写出电极A的电极方程式 , 当标况下有4.48L被处理时,通过电极B的电子数为 . 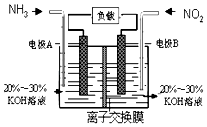
【答案】
(1)SO2、NO2
(2)K= ![]()
(3)2NH3+6e﹣+6OH﹣=N2+6H2O,0.8NA
【解析】解:(1)SO2、NO2和CO中,能和空气中的水蒸气反应的有SO2、NO2,SO2+H2O=H2SO3 H2SO3进一步被氧气氧化为硫酸,3NO2+H2O=2HNO3+NO,硫酸和硝酸融入雨水,形成酸雨,在空气中CO不能与水反应,
故答案为:SO2、NO2;
(2)反应的平衡常数表达式为生成物的浓度幂之积比上反应物浓度幂之积,所以ClO2﹣+2SO32﹣2SO42﹣+Cl﹣,平衡常数为:K= ![]() ,
,
故答案为:K= ![]() ;
;
(3)根据方程式知,6NO2+8NH3═7N2+12H2O中NO2中N元素化合价由+4价变为0价、NH3中N元素化合价由﹣3价变为0价,所以NO2发生还原反应、NH3发氧化反应,则A是负极、B是正极,负极电极方程式为2NH3﹣6e﹣+6OH﹣=N2+6H2O,所以电极A极反应式为2NH3﹣6e﹣+6OH﹣═N2+6H2O,当有4.48 L NO2 被处理时,参加反应的NO2物质的量为0.2mol,转移电子物质的量=0.2mol×[4﹣0]=0.8mol,
故答案为:2NH3+6e﹣+6OH﹣=N2+6H2O; 0.8NA.
(1)根据酸雨的形成进行回答;
(2)根据化学平衡常数的定义进行书写;
(3)根据氧化还原反应判断电极发生的反应,然后写出电极方程式,以及计算转移电子的数值.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】电子垃圾中含有大量的废弃塑料和重金属,工业上可以从电子废料(电脑主板和手机废件)中提取大量的金、银和铜,每吨电子废料中能够提取出130公斤铜,0.45公斤黄金和2公斤白银,提取流程如下:

请回答下列问题:
(1)“酸溶”过程中,王水与金反应的化学方程式为________________________。
(2)“萃取”过程中,将混合液分离所需要的主要仪器为____________________,该仪器在使用前必须进行的操作为____________________________。
(3)“还原Ⅰ”制备单质Ag的过程中,发生反应的本质是Zn和AgCl在电解质HCl中形成微电池,该过程的总反应为:2AgCl+Zn=2Ag+ZnCl2,则该电池正极的电极反应式为__________________________。
(4)滤渣的主要成分为Cu2(OH)2CO3,则“沉铜”过程中发生反应的离子方程式为______________________。
(5)滤液为NaCl、Na2CO3和NaHCO3的混合液,若上述三种物质的物质的量浓度相同,则溶液中各离子浓度的大小顺序为______________________。
(6)根据下表中数据,综合分析工业上进行“还原Ⅱ”过程中所选用的还原剂最好为______________。
物质 | 价格(元·吨-1) |
双氧水(含30%H2O2) | 3200 |
绿矾(含99.0%FeSO4·7H2O) | 1800 |
亚硫酸氢钠(含99.5%NaHSO3) | 2850 |
草酸(含99.0%H2C2O4) | 3000 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1998年6月,我国科学家参与研制的阿尔法磁谱仪随美国发现号航天飞机升入太空,开始了探索宇宙中是否存在“反物质”和“暗物质”的研究工作。根据你所学的知识推测用于制造阿尔法磁谱仪核心部件的材料是( )
A.Fe3CB.Fe3O4C.Fe2O3D.FeO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为: Fe2e===Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应aA+bB=dD+eE,若已知40g A可恰好与21g B完全反应生成28g D,则B与E的摩尔质量比为
A.7a:10dB.10a:7dC.10b:7eD.7e:11b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知分解反应2N2O5(g)![]() 4NO2(g) + O2(g)的速率方程式v = k·cm(N2O5),k是与温度有关的常数,实验测定340K时的有关数据及根据相关数据做出的图像如下:
4NO2(g) + O2(g)的速率方程式v = k·cm(N2O5),k是与温度有关的常数,实验测定340K时的有关数据及根据相关数据做出的图像如下:
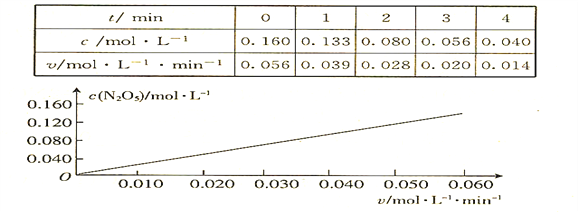
依据图表中的有关信息,判断下列有关叙述中不正确的是
A. 340K时,速率方程式中的m = 1
B. 340K时,速率方程式中的k = 0.350 min-1
C. 340K时,c(N2O5)= 0.100 mol·l-1时,v = 0.035 mol·l-1 ·min-1
D. 340K时,压强增大一倍,逆反应速率不变,正反应速率是原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。
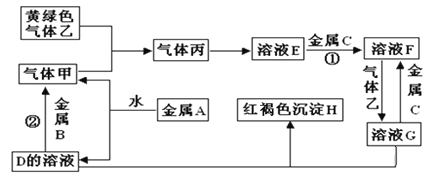
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:H_______________;乙______________。
(2)写出下列反应的离子方程式
反应①_________________________________________________________________
反应②_________________________________________________________________
(3)检验溶液G中的阳离子,可取少量溶液G于试管中,滴加KSCN溶液,现象是____________。检验溶液G中的阴离子,可另取少量溶液G于试管中,滴加__________(填化学式)溶液,现象是产生白色沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
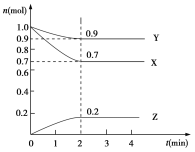
(1)起始时X的浓度为c(X)=________;反应从开始至2分钟末,Y的转化率为α(Y)=________;用Z的浓度变化表示的平均反应速率为v(Z)=________。
(2)由图中所给数据进行分析,该反应的化学方程式为______________________________。
(3)当反应进行到第___min,该反应达到平衡。此时,v(正)____v(逆) (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I﹣(aq)I3﹣(aq)某I2、KI混合溶液中,I3﹣的物质的量浓度c(I3﹣)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )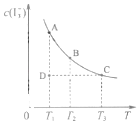
A.反应 I2(aq)+I﹣(aq)I3﹣(aq)△H>0
B.状态A与状态B相比,状态A的c(I2)大
C.若反应进行到状态D时,一定有v逆>v正
D.若温度为T1、T2 , 反应的平衡常数K1、K2则 K1>K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com