
| A、Al3+、K+、SO42-、Cl-、AlO2- |
| B、Fe2+、H+、Br-、NO3-、Cl- |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Al3+、Na+、Cl-、SO42-、NO3- |


科目:高中化学 来源: 题型:
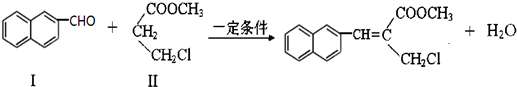
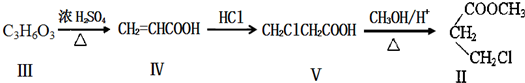
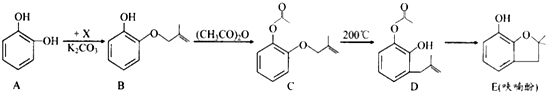
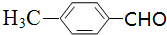 )与1分子化合物(
)与1分子化合物(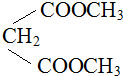 )也能发生Knoevenagel反应,则其生成的有机物的结构简式为
)也能发生Knoevenagel反应,则其生成的有机物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热盐酸溶液,溶液的pH减小 |
| B、随温度的升高,纯水的pH增大 |
| C、新制氯水经光照一段时间后,pH减小 |
| D、氢氧化钠溶液久置于空气中,pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
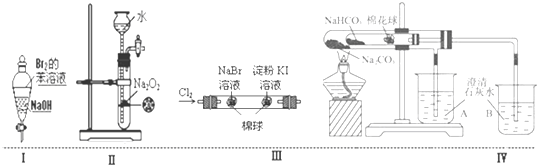
| A、实验Ⅰ:振荡后静置,溶液不再分层,且保持无色透明 |
| B、实验Ⅱ:可随关随停,随开随启控制氧气的发生 |
| C、实验Ⅲ:左边的棉球呈橙色,右边的棉球呈蓝色,证明氧化性Cl2>Br2>I2 |
| D、实验Ⅳ:小试管中NaHCO3分解,B中石灰水变浑浊,说明稳定性Na2CO3>NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
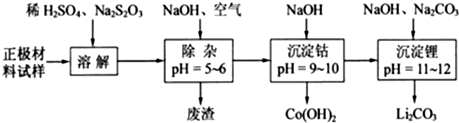
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时,容器内的压强:甲>乙 |
| B、反应达到平衡所需要的时间:甲<乙 |
| C、平衡时,氧气的浓度:甲<乙 |
| D、平衡时,容器内SO3的体积分数:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com