
| A. | 2mol/L Ba(OH)2溶液中Ba2+的物质的量和OH-的物质的量 | |
| B. | 200mL 1mol/L氯化钙溶液中c(Cl-)和100 mL 2mol/L氯化钾溶液中c(Cl-) | |
| C. | 20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度 | |
| D. | 64g二氧化硫中氧原子数和标准状况下22.4L一氧化碳中氧原子数 |
分析 A.氢氧化钡为强电解质,电离方程式:Ba(OH)2=Ba2++2OH-;
B.1 mol/L氯化钙溶液中c(Cl-)=2mol/L,2 mol/L氯化钾溶液中c(Cl-)=2mol/L;
C.氢氧化钠溶液浓度越大,密度越大,根据c=$\frac{1000ρω}{M}$判断;
D.64g二氧化硫的物质的量为1mol,含有2mol氧原子;标况下22.4L一氧化碳的物质的量为1mol,含有1mol氧原子.
解答 解:A.氢氧化钡为强电解质,电离方程式:Ba(OH)2=Ba2++2OH-,Ba2+的物质的量和OH-的物质的量之比为1:2,故A错误;
B.溶液的浓度与体积无关,1 mol/L氯化钙溶液中c(Cl-)=2mol/L,2 mol/L氯化钾溶液中c(Cl-)=2mol/L,故B错误;
C.氢氧化钠溶液浓度越大,密度越大,根据c=$\frac{1000ρω}{M}$可知,20%NaOH溶液物质的量浓度比10%NaOH溶液物质的量浓度的2倍大,故C错误;
D.64g二氧化硫的物质的量为$\frac{64g}{64g/mol}$=1mol,含有2mol氧原子;标况下22.4L一氧化碳的物质的量为1mol,含有1mol氧原子,故D正确,
故选:D.
点评 本题考查物质的量计算、物质的量浓度计算,难度不大,注意掌握物质的量浓度与质量分数之间关系.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.5 mol•L-1 | B. | 1 mol•L-1 | C. | 0.15 mol•L-1 | D. | 3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.10mL | 18.60mL |
| 第二次 | 0.30mL | 18.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:7 | C. | 7:1 | D. | 1:14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序列 | 参加反应的物质 | 生成物 |
| ① | Cl2、FeBr2 | FeCl3、FeBr3 |
| ② | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 … |
| ③ | MnO4- … | Cl2、Mn2+ … |
| A. | 第①组反应中Cl2与 FeBr2的物质的量之比为1:2 | |
| B. | 第②组反应的其余产物为H2O和 O2 | |
| C. | 氧化性由强到弱顺序MnO4->Cl2>Fe3+>Br2 | |
| D. | 第③组反应中生成1mol Cl2,转移电子2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
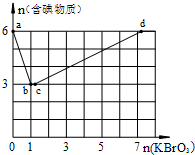 现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氢氧化钡溶液滴入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 二氧化硫与足量氢氧化钠溶液反应 SO2+2OHˉ=SO32-+H2O | |
| D. | 铝与氢氧化钠溶液反应:Al+2OH-═2A1O${\;}_{2}^{-}$+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com