
 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源:不详 题型:单选题
A.由于NaCl 晶体和CsCl晶体中正负离子半径比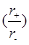 不相等,所以两晶体中离子的配位数不相等 不相等,所以两晶体中离子的配位数不相等 |
| B.CaF2晶体中,Ca2+配位数为8,F-配位数为4不相等,主要是由于F-、Ca2+电荷(绝对值)不相同 |
| C.MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大 |
| D.MCO3中M2+半径越大,MCO3热分解温度越低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子晶体中只存在非极性共价键 |
| B.稀有气体形成的晶体属于分子晶体 |
| C.干冰升华时,分子内共价键会发生断裂 |
| D.分子晶体的熔点普遍都很高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 中含有的化学键类型为 ▲ ,Fe3+与CN-之间能够形成化学键的原因是 ▲ 。
中含有的化学键类型为 ▲ ,Fe3+与CN-之间能够形成化学键的原因是 ▲ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化钠晶体中,每个晶胞中平均含有4个钠离子和4个氯离子 |
| B.在金刚石晶体中 ,1mol碳原子形成2mol碳碳共价键 |
| C.金属Po的晶体堆积模型是简单立方堆积,其配位数是8 |
| D.在干冰晶体中,每一个二氧化碳分子周围有12个二氧化碳分子紧密相邻 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属镁形成的晶体中,每个原子周围与其距离最近的原子有12个 |
| B.含有离子键的化合物形成的晶体一定是离子晶体 |
| C.原子晶体中的各相邻原子都以共价键相结合 |
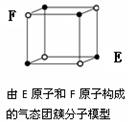
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
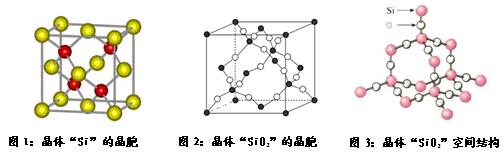
| A.金刚石>晶体硅>碳化硅 | B.K>Na>Li |
| C.NaF<NaCl<NaBr | D.CI4>CBr4>CCl4>CH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
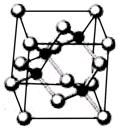
| A.砷化镓晶胞结构与NaCl相同 | B.第一电离能 As>Ga |
| C.电负性 As>Ga | D.原子半径 As>Ga |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com