
| A、H2CO3?H++HCO3-、HCO3-?H++CO32- |
| B、H2SO4?2H++SO42- |
| C、NaHCO3═Na++H++CO32- |
| D、NaHSO4═Na++H++SO42- |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原混合气体的平均组成为NO1.1 |
| B、原氨水的浓度约为17.3mol/L |
| C、吸收后氨水的浓度约为2.4mol/L |
| D、吸收后氨水的质量分数约为0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
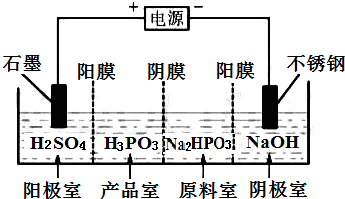 亚磷酸(H3PO3)与足量的NaOH溶液反应生成Na2HPO3.
亚磷酸(H3PO3)与足量的NaOH溶液反应生成Na2HPO3.查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:| c(CO)起始 |
| c(H2)起始 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198KJ?mol-1、P-O 360kJ?mol-1、O=O 498kJ?mol-1.则关于1mol P4和3mol O2完全反应(P4+3O2=P4O6)的热效应说法正确的是( )
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198KJ?mol-1、P-O 360kJ?mol-1、O=O 498kJ?mol-1.则关于1mol P4和3mol O2完全反应(P4+3O2=P4O6)的热效应说法正确的是( )| A、吸热1638 kJ |
| B、放热1638 kJ |
| C、放热126 kJ |
| D、吸热126 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com