
| A. | H+、Fe3+、SO42-、I- | B. | H+、NH4+、HCO3-、NO3- | ||
| C. | K+、AlO2-、Cl-、OH- | D. | Ag+、K+、Cl-、SO42- |
科目:高中化学 来源: 题型:选择题
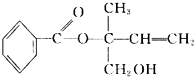
| A. | 有机物M和油脂都含有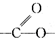 ,两者在酸性或碱性条件下都能发生取代反应 ,两者在酸性或碱性条件下都能发生取代反应 | |
| B. | M在一定条件下能发生加聚反应,不能发生酯化反应 | |
| C. | 在Ni作催化剂的条件下,1 mol M最多只能与1molH2加成 | |
| D. | 不可用酸性高锰酸钾溶液区分苯和M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①或② | C. | 只有④ | D. | ③或④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用有机溶剂从青蒿中提取青蒿素,主要采用萃取的方法 | |
| B. | 青蒿素的分子式为C15H22O5 | |
| C. | 青蒿素通过还原反应可制得双氢青蒿素 | |
| D. | 青蒿素和双氢青蒿素都是芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
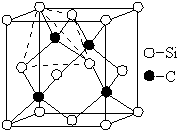 碳、氮、氟、硅、铜等元素的化合物广泛存在于自然界,回答下列问题:
碳、氮、氟、硅、铜等元素的化合物广泛存在于自然界,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com