
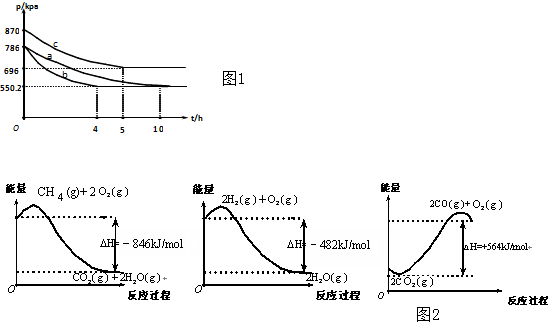
���� ��1����ѹ�����൱�ں���������ѹ����ƽ�������ƶ���
��2�����ݵ���ƽ����ʱ�Ķ��ٿ��ԱȽϳ���Ӧ���ʵĴ�С���ٸ���ͼ���е����ߵı仯�����жϳ������ĸı䣻��������������ѹǿ֮�Ⱦ͵������ʵ���֮�ȣ��������ת���ʣ�
��3�������Ȼ�ѧ����ʽ��˹���ɼ���õ������Ȼ�ѧ����ʽ��
��4�����ݻ�ѧ��Ӧ�ı����Ǿɼ��Ķ��Ѻ��¼����γɷ��������¶Ⱥ�ѹǿ�ĽǶȿ��ǣ�
��� �⣺��1����֪N2+3H2?2NH3���÷�Ӧ�����������С�ķ�Ӧ����ͬ�¶��£��ֱ�1molN2��3molH2���ں�ѹ������ͺ����������У���������ʼ�ݻ���ͬ����ַ�Ӧ��
��ѹ�����൱�ں���������ѹ����ƽ�������ƶ������Ժ�ѹ��������NH3������������ں���������
�ʴ�Ϊ������
��2�����ݵ�abc��ƽ����ʱ�Ķ��ٿ��ԱȽϳ���Ӧ���ʵĴ�СΪ��b��c��a����a��ȣ�cʵ�鵽��ƽ��ʱ��ѹǿ���˵��ƽ�������ƶ�������ѧ��Ӧ���ʱ���ǵ��÷�Ӧ�Ƿ��ȷ�Ӧ�������������¶������µģ�����ѹǿ֮�Ⱦ͵������ʵ���֮�ȣ�ʵ��b��N2��ƽ��ת����Ϊ��$\frac{786-550.2}{786}$��100%=30%��
�ʴ�Ϊ��bca�������¶ȣ�30%��
��3����ͼ2��֪��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-846KJ/mol ��
2H2��g��+O2��g��=2H2O��g����H=-482KJ/mol��
2CO��g��+O2��g��=2CO2��g����H=+564KJ/mol��
��[�١�2-�ڡ�3-��]��$\frac{1}{2}$�ɵã�CH4��g��+H2O��g��=CO��g��+3H2��g����H=[��-846��KJ/mol����2-��-482KJ/mol ����3-��+546KJ/mol ��]��$\frac{1}{2}$=+159 kJ/mol������CH4��g����H2O��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ����ʽΪCH4��g��+H2O��g��=3H2��g��+CO��g����H=+159 kJ/mol��
�ʴ�Ϊ��CH4��g��+H2O��g��=3H2��g��+CO��g����H=+159 kJ/mol��
��4���ڵ�ų��������µ��������������ѣ������˷�Ӧ����Ҫ����������Ӧ�������У���ͳ�ĺϳɰ��������Ǹ��¡���ѹ���÷������ŵ��ǵ��¡���ѹ�������ͽ�Լ����Դ�������˶��豸��Ҫ��
�ʴ�Ϊ����ų��������µ������������ѣ������˷�Ӧ�����ܣ���Ӧ���������ܼ��ţ��������豸Ҫ��
���� ���⿼���˻�ѧƽ���й�֪ʶ��ע����շ�Ӧ��ԭ�����ؼ���Ҫѧ������ȷ����Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ������أ�����������ѧ����������������ͽ��������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A��B��C��D | B�� | C��A��D��B | C�� | A��C��D��B | D�� | B��D��C��A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ������̼ | C�� | ú | D�� | ̼�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 200mL 1mol/L��NaCl��Һ | B�� | 150 mL 1mol/L��MgCl2��Һ | ||
| C�� | 100mL 1mol/L��HCl��Һ | D�� | 50mL 1mol/L��AlCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH2-CH2-COOH | |
| B�� | NH2-CH2-CH2OH | |
| C�� | 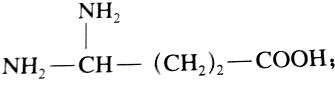 | |
| D�� | 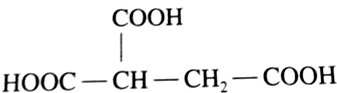 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
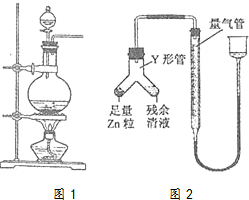 ʵ���ҳ���MnO2��Ũ���ᷴӦ�Ʊ�Cl2����Ӧװ����ͼ1��ʾ��
ʵ���ҳ���MnO2��Ũ���ᷴӦ�Ʊ�Cl2����Ӧװ����ͼ1��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | �����Լ� | ʵ������ |
| �� | 2�� 0.1mol/L��FeCl3����Һ | �ٰ�ɫ����ת��Ϊ���ɫ���� |
| �� | 4mL2mol/LNH4Cl��Һ | �ڰ�ɫ�����ܽ⣬����ɫ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3CH2OH+CH3COOH��$?_{��}^{Ũ����}$CH3COOCH2CH3+H2O | |
| B�� | CH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O | |
| C�� | 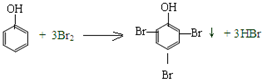 | |
| D�� | CH3CH2OH+HBr$\stackrel{��}{��}$CH3CH2Br+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5.6 g������0.1mol�����г��ȼ�գ�ת�Ƶ�����Ϊ0.3NA | |
| B�� | 2.5mL 16mol•L-1Ũ����������ͭ��Ӧ��ת�Ƶ�����Ϊ0.04NA | |
| C�� | 7.8g Na2S��Na2O2�Ĺ��������к��е�������������0.1NA | |
| D�� | �����£�5.6 g ����������Ũ���ᷴӦ��ת�Ƶĵ�����Ϊ0.3 NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com