
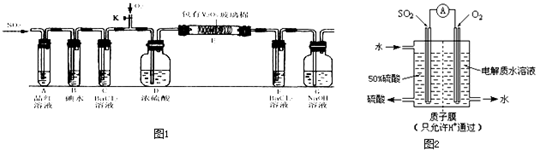
 2SO3;二氧化硫有毒,且是大气硫酸型酸雨的主要成分,需进行尾气处理,装置G的作用为吸收尾气中的SO2,防止污染空气,
2SO3;二氧化硫有毒,且是大气硫酸型酸雨的主要成分,需进行尾气处理,装置G的作用为吸收尾气中的SO2,防止污染空气, 2SO3;吸收尾气中的SO2,防止污染空气;
2SO3;吸收尾气中的SO2,防止污染空气; 

科目:高中化学 来源: 题型:
(16分) 硫及其化合物有如下转化关系
(1)发生氧化还原反应的是 (填序号)
(2)写出(5)的反应方程式 ,
说明浓硫酸具有 ,制取CuSO4, 方法最好(填序号),
(3)SO2是造成空气污染,形成酸雨的主要物质。SO2在水的存在下与氧气反应生成硫酸,反应方程式为 。
验证二氧化硫的方法是 。
(4)某溶液中含有Cl-、SO42-,可能含有Na+、Fe2+或其中一种。
①验证Cl-、SO42-的方法是
A.先加BaCl2溶液,等沉淀后,再加AgNO3溶液
B.先加AgNO3溶液,等沉淀后,再加BaCl2溶液
C.先加Ba(NO3)2溶液,等沉淀后,再加AgNO3溶液
②验证Na+或Fe2+最简单的方法是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省陕师大附中高一上学期期末试题化学(理)试卷 题型:填空题
(16分)硫及其化合物有如下转化关系
(1)发生氧化还原反应的是 (填序号)
(2)写出(5)的反应方程式 ,
说明浓硫酸具有 ,制取CuSO4, 方法最好(填序号),
(3)SO2是造成空气污染,形成酸雨的主要物质。SO2在水的存在下与氧气反应生成硫酸,反应方程式为 。
验证二氧化硫的方法是 。
(4)某溶液中含有Cl-、SO42-,可能含有Na+、Fe2+或其中一种。
①验证Cl-、SO42-的方法是
A.先加BaCl2溶液,等沉淀后,再加AgNO3溶液
B.先加AgNO3溶液,等沉淀后,再加BaCl2溶液
C.先加Ba(NO3)2溶液,等沉淀后,再加AgNO3溶液
②验证Na+或Fe2+最简单的方法是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山西省四校高三第二次联考化学试卷(解析版) 题型:填空题
(8分)最近雾霾天气又开始肆虐我国大部分地区。其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该吸收反应的离子方程式是
(2)已知H2SO3的电离常数为 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的电离常数为 K1=4.30×10-7, K2= 5.60×10-11,则下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣):n(HSO3﹣)变化关系如下表:
|
n(SO3²﹣):n(HSO3﹣) |
91 :9 |
1 :1 |
1 :91 |
|
pH |
8.2 |
7.2 |
6.2 |
①上表判断NaHSO3溶液显 性,从原理的角度解释原因
②在NaHSO3溶液中离子浓度关系不正确的是(选填字母):
A.(Na+)= 2c(SO32-)+ c(HSO3-),
B.(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-),
C.(H2SO3)+ c(H+)= c(SO32-)+ (OH-),
D.(Na+)+ c(H+)= 2 c(SO32-)+ c(HSO3-)+ c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生 。再生示意图如下:

① 吸收液再生过程中的总反应方程式是 。
② 当电极上有1mol电子转移时阴极产物为 克.
查看答案和解析>>
科目:高中化学 来源:2014届陕西省高一上学期期末试题化学(理)试卷 题型:填空题
(16分) 硫及其化合物有如下转化关系
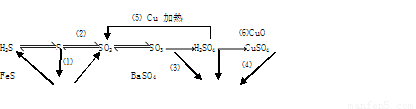
(1)发生氧化还原反应的是 (填序号)
(2)写出(5)的反应方程式 ,
说明浓硫酸具有 ,制取CuSO4, 方法最好(填序号),
(3)SO2是造成空气污染,形成酸雨的主要物质。SO2在水的存在下与氧气反应生成硫酸,反应方程式为 。
验证二氧化硫的方法是 。
(4)某溶液中含有Cl-、SO42-,可能含有Na+、Fe2+或其中一种。
①验证Cl-、SO42-的方法是
A.先加BaCl2溶液,等沉淀后,再加AgNO3溶液
B.先加AgNO3溶液,等沉淀后,再加BaCl2溶液
C.先加Ba(NO3)2溶液,等沉淀后,再加AgNO3溶液
②验证Na+或Fe2+最简单的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com