
| SO2(g) | O2(g) | SO3(g) | |
| 初始浓度(mol?L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L-1) | c1 | c2 | 0.4 |
| A、反应前5min内,用SO2表示的平均速率为0.04mol?L-1?min-1 |
| B、其他条件不变,若增大SO2的浓度,则达平衡时SO2转化率会增大 |
| C、降低温度,其他条件不变,平衡时n(SO2)=3.0mol,则反应的△H<0 |
| D、平衡后移走2.0mol SO2和1.0mol O2,在相同条件下再达新平衡时,c(SO3)<0.2mol?L-1 |
| 0.4 |
| 5 |
| 0.4 |
| 5 |
| 0.4 |
| 5 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、反应进行30 s时,正反应速率等于逆反应速率 |
| B、反应进行80 s时,逆反应速率大于正反应速率 |
| C、反应进行60 s时,X的物质的量浓度为0.04 mol/L |
| D、反应进行60 s时,Y的转化率为70% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+ |
| B、Al(OH)3 |
| C、AlO2- |
| D、Al3+和Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、.新型能源生物柴油和矿物油主要化学成分相同 |
| B、.“洁厕灵”有效成分为盐酸,与漂白粉混合使用效果更佳 |
| C、静置后的淘米水能产生丁达尔现象,这种“淘米水”是胶体 |
| D、.铝热反应中可得到铁,工业上可以利用该反应来大量生产铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱难溶于水 |
| B、纯碱是碱而不是盐 |
| C、纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 |
| D、纯碱中含有少量的小苏打可以用稀盐酸除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 纯净物 | 混合物 | 弱电解质 | 非电解质 |
| A | 明矾 | 蔗糖 | NaHCO3 | CO2 |
| B | 天然橡胶 | 石膏 | SO2 | CH3CH2OH |
| C | 冰 | 王水 | H2SiO3 | Cl2 |
| D | 胆矾 | 玻璃 | H2CO3 | NH3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
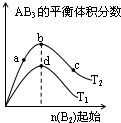 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )| A、若T2>T1,则正反应一定是放热反应 |
| B、达到平衡时A2的转化率大小为:b>a>c |
| C、若T2>T1,达到平衡时b、d点的反应速率为vd>vb |
| D、在T2和n(A2)不变时达到平衡,AB3的物质的量大小为:c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有最低价元素的化合物不一定具有很强的还原性 |
| B、元素的单质一定是由氧化或还原该元素的化合物制得 |
| C、阳离子只能得电子被还原,阴离子只能失电子被氧化 |
| D、在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m+n>p+q,正反应是放热反应 |
| B、m+n>p+q,正反应是吸热反应 |
| C、m+n<p+q,逆反应是放热反应 |
| D、m+n>p+q,逆反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com