
 2007年诺贝尔物理学奖为法国科学家阿尔贝•费尔和德国科学家彼得•格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就.某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应.
2007年诺贝尔物理学奖为法国科学家阿尔贝•费尔和德国科学家彼得•格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就.某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应. .
.分析 (1)利用均摊法计算晶体晶胞中氢所各原子的个数,再根据原子数之比确定化学式;
(2)根据化合价代数和为0的原则计算;
(3)Mn的原子序数为27,根据核外电子排布规律写出核外外围电子轨道表示式;
(4)A.根据元素在周期表中的位置判断;
B.CaO为离子晶体;
C.图中堆积方式为镁型;
D.元素的电负性越强,金属性越弱.
解答 解:(1)由图1可知,晶胞中A位于顶点,晶胞中含有A为$8×\frac{1}{8}$=1个,B位于晶胞的体心,含有1个,O位于面心,晶胞中含有O的个数为6×$\frac{1}{2}$=3,则化学式为ABO3,
故答案为:ABO3;
(2)设La1-xAxMnO3中三价锰与四价锰的物质的量分别为m和n,则有 $\left\{\begin{array}{l}{3(1-x)+2x+3m+4n=6}\\{m+n=1}\end{array}\right.$,解得m=1-x,n=x,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为$\frac{1-x}{x}$,
故答案为:$\frac{1-x}{x}$;
(3)Mn的原子序数为27,外围电子轨道表示式为 ,故答案为:
,故答案为: ;
;
(4)A.由元素在周期表中的位置可知镧、锰、氧分别位于周期表f、d、p区,故A正确;
B.O、N元素都是第二周期非金属元素,同一周期元素自左而右第一电离能呈增大趋势,但N元素原子2p能级是半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故B错误;
C.图中堆积方式为镁型,故C错误;
D.元素的电负性越强,金属性越弱,故D正确.
故答案为:AD.
点评 本题考查较为综合,主要考查了晶胞的计算、核外电子排布、第一电离能、电负性等知识点,题目难度中等,注意利用均摊法计算晶胞的构成.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:选择题
| A. | ZnCl2 | B. | KCl | C. | NaCl | D. | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯铜作阳极,含Zn、Ag的Cu合金作阴极 | |
| B. | 含Zn、Ag的Cu合金作阳极,纯铜作阴极 | |
| C. | 用纯铁作阳极,纯铜作阴极 | |
| D. | 用石墨作阳极,用惰性电极(Pt)作阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
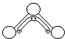 1949年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家.O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图所示:呈V型,键角116.5°.三个O原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键(虚线内部分)-三个O原子均等地享有这4个电子.请回答:
1949年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家.O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图所示:呈V型,键角116.5°.三个O原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键(虚线内部分)-三个O原子均等地享有这4个电子.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
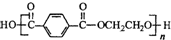 ,外用材料是纯羊毛线.则下列有关说法不正确的是( )
,外用材料是纯羊毛线.则下列有关说法不正确的是( )| A. | 羊毛的主要成分属于蛋白质 | |
| B. | 涤纶属于天然高分子化合物 | |
| C. | 合成涤纶的单体之一可以是HOCH2CH2OH | |
| D. | 可用灼烧的方法区别羊毛和涤纶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com