
有关水的电离平衡的说法正确的是( )
| A.水的离子积通常用KW来表示,随温度变化而变化,只适用于纯水,在稀盐酸中数值会变大 |
| B.在纯水中加入硫酸会抑制水的电离,加醋酸会促进水的电离 |
| C.盐溶于水对水的电离平衡均没有影响 |
| D.在纯水中加入氢氧化铁固体对水的电离平衡会有微弱的影响 |
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:单选题
下列说法不正确的是
| A.加热或稀释NH4Cl溶液,NH4Cl水解程度均增大 |
| B.滴有酚酞试液的氨水中加入NH4Cl固体,溶液颜色变浅 |
| C.含有NH4Cl的氨水中,[NH4+]可能大于[Cl-] |
| D.纯水中加入少量NH4Cl固体,恢复到原温度,水的电离平衡右移且电离常数变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:
K2SO4·MgSO4·2CaSO4(s) 2Ca2++2K++Mg2++4SO42-,不同温度下,K+的浸出浓度与溶浸时间的关系如右图所示,则下列说法错误的是
2Ca2++2K++Mg2++4SO42-,不同温度下,K+的浸出浓度与溶浸时间的关系如右图所示,则下列说法错误的是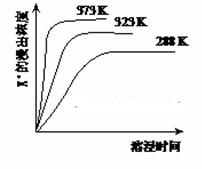
| A.向该体系中加入饱和NaOH溶液,溶解平衡向右移动 |
| B.向该体系中加入饱和碳酸钠溶液,溶解平衡向右移动 |
| C.升高温度,反应速率增大,平衡向正反应方向移动 |
| D.该平衡的Ksp= c(Ca2+) ·c(K+)·c(Mg2+)·c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,向100 mL 0.1 mol·L-1 H2A(二元酸)溶液中逐滴加入0.2 mol·L-1 NaOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列有关说法正确的是( )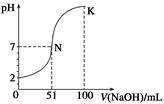
| A.H2A为二元强酸 |
| B.N点对应溶液有:c(Na+)=c(A2-)+c(HA-) |
| C.K点对应溶液中离子浓度由大到小的顺序为c(A2-)>c(Na+)>c(OH-)>c(H+) |
| D.K点时加水稀释溶液,c(H+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见下图。下列说法正确的是 ( )
| A.在任何溶液中,c(Ca2+)、c(SO42—)均相等 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42—)一定等于3×10-3mol·L-1 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.d点溶液通过蒸发可以变到c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是 ( )
①将水加热煮沸 ②向水中投入一小块金属钠 ③向水中通CO2 ④向水中加入NH4Cl固体 ⑤向水中加入NaHCO3固体 ⑥向水中加入NaHSO4固体
| A.①②⑤ | B.①④ | C.③④⑥ | D.④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用水稀释0.1 mol·L-1氨水时,溶液中随水量的增加而减小的是 ( )。
| A.c(OH-)/c(NH3·H2O) |
| B.c(NH3·H2O)/c(OH-) |
| C.n(OH-)和c(H+) |
| D.c(H+)和c(OH-)的乘积 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某同学取等体积的稀盐酸与稀醋酸各一份进行稀释,下面是稀释前后的有关数据及结论,其中肯定错误的是 ( )
| | A | B | C | D |
| 稀释前 | 酸浓度相同 | 酸浓度相同 | pH均为3 | pH均为3 |
| 稀释量 | 均为10倍 | 稀释至两酸pH相同 | 稀释至pH均为5 | 均为100倍 |
| 结论 | pH:盐酸的小 | 稀释倍数:盐酸的大 | 稀释倍数:盐酸的大 | pH:盐酸的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温下,取0.3 mol·L-1HY溶液与0.3 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是 ( )
| A.混合溶液中由水电离出的c(OH-)=10-9 mol·L-1 |
| B.溶液中离子浓度由大到小的顺序为c(Y-)>c(Na+)>c(OH-)>c(H+) |
| C.混合溶液中c(Na+)=c(Y-)+c(HY)=0.3 mol·L-1 |
| D.混合溶液中c(OH-)-c(HY)=c(H+)=1×10-9 mol·L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com