
【题目】开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)催化反应室中的总反应3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K=
CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K=![]() ,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L-1,c(H2)=1.4mol·L-1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为___。
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
c(mol·L-1) | 0.46 | 1.0 | 1.0 |
此时刻v正___v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___。
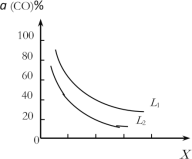
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
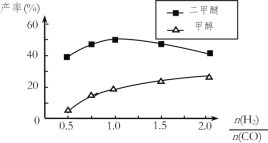
(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比![]() 的改变二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
的改变二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
【答案】-262.7kJ·mol-1 C(s)+H2O(g)![]() H2(g)+CO(g) △H=+131.3kJ·mol-1 0.075mol·L-1·min-1 > 1.2mol·L-1 温度 > 当投料比大于1时,随着c(H2)增大,反应①被促进,而反应③被抑制,c(H2O)增大,最终抑制反应②,因此甲醇的产率继续增大而二甲醚的产率减小
H2(g)+CO(g) △H=+131.3kJ·mol-1 0.075mol·L-1·min-1 > 1.2mol·L-1 温度 > 当投料比大于1时,随着c(H2)增大,反应①被促进,而反应③被抑制,c(H2O)增大,最终抑制反应②,因此甲醇的产率继续增大而二甲醚的产率减小
【解析】
(1)将反应①、②、③联立可得催化反应室中总反应化学方程式,根据盖斯定律便可计算H;根据煤的气化平衡常数表达式以及质量守恒,可写出该反应的化学方程式,根据生成1molH2需要吸收131.3kJ的热量可算出反应热;
(2)根据反应①中CO、H2的起始浓度和CO的转化率用三段式可计算H2的浓度变化,再利用题给时间可求出8min内H2的平均反应速率;
(3)先计算浓度商,将计算结果与化学平衡常数相比确定反应方向,从而确定正逆反应速率相对大小;根据化学平衡常数可计算平衡时二甲醚的物质的量浓度;
(4)根据催化反应室的总反应放热化学方程式可知CO的平衡转化率a(CO)与温度、压强的关系,从而判断X是温度还是压强,并判断L1、L2的相对大小;
(5)根据平衡移动原理分析起始投料比![]() 的改变如何直接或间接影响反应①、②、③,对照图中曲线变化,可推测投料比大于1.0之后二甲醚产率和甲醇产率变化的原因。
的改变如何直接或间接影响反应①、②、③,对照图中曲线变化,可推测投料比大于1.0之后二甲醚产率和甲醇产率变化的原因。
(1)催化反应室中的总反应3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)可按以下方法联立得到:①×2+②+③,根据盖斯定理,该反应△H=-99kJ·mol-1×2+(-23.5kJ·mol-1)+ (-41.2kJ·mol-1)= -262.7kJmol-1;根据煤的气化平衡常数表达式以及质量守恒,可写出该反应的化学方程式为:H2O(g)+C(s)
CH3OCH3(g)+CO2(g)可按以下方法联立得到:①×2+②+③,根据盖斯定理,该反应△H=-99kJ·mol-1×2+(-23.5kJ·mol-1)+ (-41.2kJ·mol-1)= -262.7kJmol-1;根据煤的气化平衡常数表达式以及质量守恒,可写出该反应的化学方程式为:H2O(g)+C(s)![]() H2(g)+CO(g),根据生成1molH2需要吸收131.3kJ的热量可知该反应的△H=+131.3kJmol-1,则该反应的热化学方程式为:C(s)+H2O(g)
H2(g)+CO(g),根据生成1molH2需要吸收131.3kJ的热量可知该反应的△H=+131.3kJmol-1,则该反应的热化学方程式为:C(s)+H2O(g)![]() H2(g)+CO(g) △H=+131.3kJ·mol-1。
H2(g)+CO(g) △H=+131.3kJ·mol-1。
答案为:-262.7kJmol-1;C(s)+H2O(g)![]() H2(g)+CO(g) △H=+131.3kJ·mol-1;
H2(g)+CO(g) △H=+131.3kJ·mol-1;
(2)根据题给数据,CO的反应量为0.6mol/L×50%=0.3mol/L,则有:

则8min内H2的平均反应速率为:v (H2)= ![]() =0.075molL-1min-1。
=0.075molL-1min-1。
答案为:0.075molL-1min-1;
(3)该时刻反应的浓度熵为:Qc = ![]() <400,平衡正向移动,所以,v正>v逆;
<400,平衡正向移动,所以,v正>v逆;
设平衡时CH3OCH3物质的量浓度为x,则有:

x=0.2mol/L,则平衡时c(CH3OCH3) =1mol/L +0.2mol/L=1.2mol/L。
答案为:>;1.2mol/L;
(4)根据催化反应室的总反应放热化学方程式3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g) △H= -262.7kJmol-1,可知,正向反应气体减少,反应放热。所以,CO的平衡转化率a(CO)随温度的升高而减小、随压强的增大而增大,图中曲线随X增大而减小,可判断X是温度,则L1、L2是压强,且L1>L2。
CH3OCH3(g)+CO2(g) △H= -262.7kJmol-1,可知,正向反应气体减少,反应放热。所以,CO的平衡转化率a(CO)随温度的升高而减小、随压强的增大而增大,图中曲线随X增大而减小,可判断X是温度,则L1、L2是压强,且L1>L2。
答案为:温度;>;
(5)结合图象,根据平衡移动原理随着![]() 增大,反应①CO转化率增大,甲醇的产率增大,进而有利于反应②正向移动;另一方面,随着
增大,反应①CO转化率增大,甲醇的产率增大,进而有利于反应②正向移动;另一方面,随着![]() 增大,反应③被抑制,c(H2O)增大,进而抑制了反应②;图中二甲醚产率随着
增大,反应③被抑制,c(H2O)增大,进而抑制了反应②;图中二甲醚产率随着![]() 增大先增大后减小的原因就是这两种因素共同作用的结果:当投料比小于1时,以前一因素影响为主;当投料比大于1时,以后一因素影响为主。总之,题给图中投料比大于1.0之后二甲醚产率和甲醇产率变化的原因可解释为:当投料比大于1时,随着c(H2)增大,反应①被促进,而反应③被抑制,c(H2O)增大,最终抑制反应②,因此甲醇的产率继续增大而二甲醚的产率减小。
增大先增大后减小的原因就是这两种因素共同作用的结果:当投料比小于1时,以前一因素影响为主;当投料比大于1时,以后一因素影响为主。总之,题给图中投料比大于1.0之后二甲醚产率和甲醇产率变化的原因可解释为:当投料比大于1时,随着c(H2)增大,反应①被促进,而反应③被抑制,c(H2O)增大,最终抑制反应②,因此甲醇的产率继续增大而二甲醚的产率减小。
答案为:当投料比大于1时,随着c(H2)增大,反应①被促进,而反应③被抑制,c(H2O)增大,最终抑制反应②,因此甲醇的产率继续增大而二甲醚的产率减小。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】下列关于电化学的说法中错误的是( )
A.原电池的负极、电解池的阳极均发生氧化反应
B.原电池将化学能转化为电能,电解池将电能转化为化学能
C.利用原电池原理可制备化学电源,利用电解池原理可制备化学物质
D.电解水制取H2和O2时,为了增强导电性,可加入NaCl、H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是
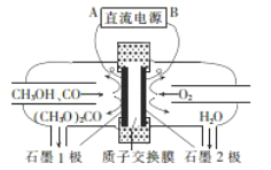
A. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l:2
B. 石墨l极发生的电极反应为2CH3OH+CO-e-=(CH3O)2CO+H+
C. 石墨2极与直流电源正极相连
D. H+由石墨2极通过质子交换膜向石墨l极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.pH=l的溶液中:Ba2+、Fe3+、Cl-、SCN-
B.能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32-
C.![]() =10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D.由水电离的c(H+)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二镍(Ni2O3)可用于制造高能电池元件。电解法制备过程如下:用NaOH 溶液将NiCl2溶液的pH调至7.5(该pH下溶液中的Ni2+不沉淀),加入适量硫酸钠固体后进行电解。电解过程中产生的Cl2(不考虑Cl2的逸出)在弱碱性条件下生成ClO﹣,ClO﹣再把二价镍(可简单写成Ni2+)氧化为Ni3+,再将Ni3+经一系列反应后转化为Ni2O3,电解装置如图所示。下列说法不正确的是( )

A. 加入适量硫酸钠的作用是增加离子浓度,增强溶液的导电能力
B. 电解过程中阴、阳两极附近溶液的pH均升高
C. 当有1mol Ni2+氧化为Ni3+时,外电路中通过的电子数目为1NA,通过阳离子交换膜的Na+数目为1NA
D. 反应前后b池中Cl- 浓度几乎不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应CO2(g)+C(s)![]() 2CO(g)的△H<0,△S>0
2CO(g)的△H<0,△S>0
B. 钢铁水闸可用牺牲阳极或者外加电流的阴极保护法减缓其腐蚀
C. 常温下,KSP[Al(OH)3]=1×10-33。欲使溶液中c(Al3+)≤1×10-6 mol·L-1,需调节溶液的pH≥5
D. 常温常压下,11.2 L Cl2与足量铁粉充分反应,转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )

A. 由 图甲可知,a点Kw的数值比b点Kw的数值大
B. 乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH<0
C. 丙表示0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】页岩气中含有较多的乙烷,可将其转化为更有工业价值的乙烯。
(1) 二氧化碳氧化乙烷制乙烯。
将C2H6和CO2按物质的量之比为1∶1通入反应器中,发生如下反应:
ⅰ.C2H6(g) ![]() C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol 1
C2H4(g) + H2(g) ΔH1=+136.4 kJ·mol 1
ⅱ.CO2(g) + H2(g) ![]() CO(g) + H2O(g) ΔH2=+41.2 kJ·mol 1
CO(g) + H2O(g) ΔH2=+41.2 kJ·mol 1
ⅲ.C2H6(g) +CO2(g) ![]() C2H4(g) +CO(g) +H2O(g) ΔH3
C2H4(g) +CO(g) +H2O(g) ΔH3
①用ΔH1、ΔH2计算ΔH3=______kJ·mol1。
②反应ⅳ:C2H6(g) ![]() 2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:__。
2C(s)+3H2(g)为积碳反应,生成的碳附着在催化剂表面, 降低催化剂的活性,适当通入过量 CO2 可以有效缓解积碳,结合方程式解释其原因:__。
③二氧化碳氧化乙烷制乙烯的研究热点之一是选择催化剂,相同反应时间,不同温度、不同催化剂的数据如下表(均未达到平衡状态):

(注)C2H4 选择性:转化的乙烷中生成乙烯的百分比。
CO 选择性:转化的 CO2 中生成 CO 的百分比。
对比Ⅰ和Ⅱ,该反应应该选择的催化剂为__,理由是__。实验条件下,铬盐作催化剂时,随温度升高,C2H6 的转化率升高,但 C2H4 的选择性降低,原因是__。
(2) 利用质子传导型固体氧化物电解池将乙烷转化为乙烯,示意图如图:
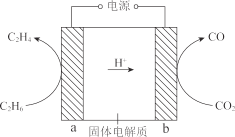
①电极 a 与电源的______极相连。
②电极 b 的电极反应式是 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
① 2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH1<0 平衡常数为K1;
2ClNO(g) ΔH1<0 平衡常数为K1;
② 2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;
NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:_________________。ΔH3=__________(用ΔH1、ΔH2表示)。
2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:_________________。ΔH3=__________(用ΔH1、ΔH2表示)。
(2)①为研究不同条件对反应①的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应①达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=______mol,NO的转化率α1=______。
②其他条件保持不变,反应②升高温度,平衡时NO2的转化率_____((填“增大”“减小”或“不变”),平衡常数K2______(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com