
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 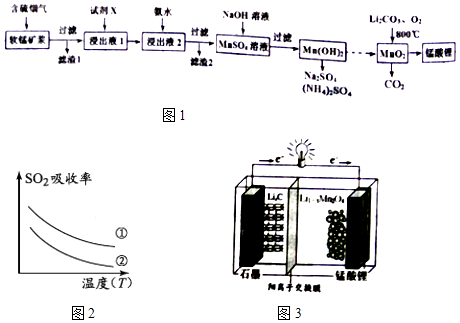
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.
【答案】
(1)ad
(2)H2O2
(3)除去铁、铝元素
(4)Li1﹣xMnO4+xLi++xe﹣=LiMn2O4;7
【解析】解:(1)a.降低通入含硫烟气的温度,可提高SO2吸收率.a正确;b.升高通入含硫烟气的温度,不能提高SO2吸收率.b错误;c.减少软锰矿浆的进入量,不能提高SO2吸收率.c错误;d.减小通入含硫烟气的流速,可提高SO2吸收率.d正确.所以答案是:ad;(2)将亚铁离子氧化成铁离子,应选择H2O2 , 所以答案是:H2O2;(3)加氨水调溶液pH在5~6之间,使Fe3+、Al3+阳离子转化为氢氧化铁、氢氧化铝沉淀而除去,所以答案是:除去铁、铝元素;(4)①根据总反应式可知Li失去电子,电池负极反应式为:xLi﹣xe﹣═xLi+ , 由总反应式减去负极反应式可得放电时的正极反应式为Li1﹣xMnO4+xLi++xe﹣═LiMnO4 , 所以答案是:Li1﹣xMnO4+xLi++xe﹣═LiMnO4;
②充电时,若转移1mole﹣ , 则石墨电极上产生1molLi,质量为1mol×7g/mol=7g,
所以答案是:7.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,甲烷的燃烧热是890.3kJmol﹣1 , 则下列热化学方程式书写正确的是( )
A.CH4(g)+ ![]() O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
O2(g)═CO(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
B.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3kJ?mol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3kJ?mol﹣1
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质。下列判断正确的是
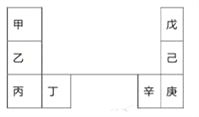
A. 金属性:甲>乙>丁 B. 原子半径:辛>己>戊
C. 丙和庚的原子核外电子数相差11 D. 乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】nmolO2与nmolCO相比较,下列说法不正确的是( )
A. 在同温同压下体积相等
B. 原子数相等
C. 在标准状况下质量相等
D. 分子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蒸馏操作的有关叙述不正确的是 ( )
A.蒸馏操作的主要仪器是:蒸馏烧瓶、酒精灯、铁架台、冷凝管、锥形瓶、牛角管、温度计等
B.蒸馏操作使用的温度计的水银球应插入到液体内
C.在蒸馏烧瓶内放入少量碎瓷片,目的是防止暴沸
D.冷凝管进出水的方向是下口进、上口出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工农业生产中应用广泛.
(1)基态硼原子的核外电子排布式为 , 有种不同能量的电子.
(2)BF3溶于水后.在一定条件下可转化为H3O+[B(OH)F3]﹣ , 该物质中阳离子的空间构型为 , 阴离子的中心原子轨道采用杂化.
(3)与BH4﹣互为等电子休的分子是(写化学式).
(4)EminBF4的熔点为12℃,在常温下为液体,由有机物阳离子[Emin]+和[BF4]﹣构成.该物质的晶体属于晶体.
(5)一种由硼和钐(Sm)形成的晶体的晶胞结构如图所示,已知晶胞常数a=n pm,则晶体的密度为gcm﹣3(设NA为阿伏伽德罗常数的值). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】准确称取6.0 g铝土矿样品(主要成分为Al2O3,含Fe2O3杂质),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )

A. 3.50 mol·L-1
B. 1.75 mol·L-1
C. 0.85 mol·L-1
D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列8种化学符号:168O2、188O2、H、126C、![]() Na、
Na、![]() 7N、146C、
7N、146C、![]() Mg。
Mg。
(1)表示核素的符号共________种。
(2)互为同位素的是______________。
(3)质量相同的H![]() O和D
O和D![]() O所含中子数之比为________。
O所含中子数之比为________。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2 [Be(OH) 4]的离子方程式__________________。
(5)Be(OH) 2与Mg(OH)2可用_______________试剂鉴别。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com