
| A. | N2O和CO2 | B. | O3和NO2 | C. | CH4和NH3 | D. | OH-和NH2 |
分析 具有相同原子数和电子数的微粒互称为等电子体,据此对各选项进行判断.
解答 解:A.N2O和CO2,原子数目都为3个,电子数分别为:7×2+8=22,6+8×2=22,属于等电子体,故A正确;
B.O3和NO2,原子数目都为3个,电子数分别为:8×3=24,7+8×2=23,不属于等电子体,故B错误;
C.CH4和NH3,原子数目不同,不属于等电子体,故C错误;
D、OH-和NH2,原子数目不相同,电子数分别为:16+1+1=18,14+1×2=16,不属于等电子体,故D错误;
故选A.
点评 本题考查了等电子原理的应用,题目难度不大,明确等电子体的概念为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | x=3 y=l | B. | x=4 y=1 | C. | x=5 y=1 | D. | x=2 y=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
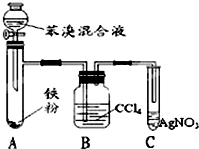 如表是A、B、C三种烃的有关信息;
如表是A、B、C三种烃的有关信息;| A | B | C |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  | 1棍模型为: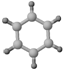 ②平面型结构 | ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与H2在一定条件下反应生成A |
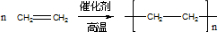 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的比例模型: | |
| B. | N2H4的电子式为: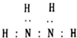 | |
| C. | NaH中氢离子结构示意图为: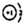 | |
| D. | 质子数是82,中子数是122的铅原子:${\;}_{82}^{122}$Pb |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ④⑤⑥ | D. | ②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
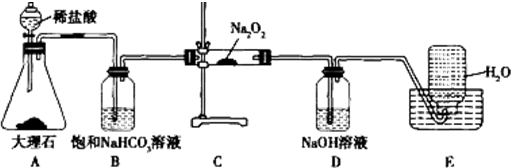
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com