
���� I����1��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��ǿ���ܺ������η�Ӧ�������
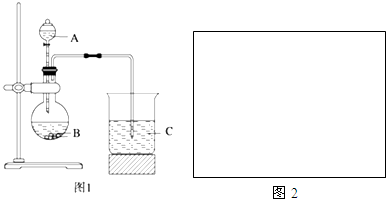
��2����ϡ�����̼���Ʒ�Ӧ��ȡ������̼���ö�����̼��ˮ��������Һ��Ӧ��ȡ���
��3���ձ�C�з�����Ӧ�����ӷ���ʽΪ������̼��ˮ��������ӷ�Ӧ����̼������Ӻ��
��4�����ж�����ǿ�����жϷǽ�����ǿ����
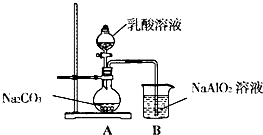
II����1��C��������������Һ��Ӧ���ɵ�����
��2�������������ӷ�Ӧ����������������ӣ�
��3�������ж�������Ⱦ������
III����1�������Ľ�����ǿ�����жϷ����У�����֮����û���Ӧ��������ˮ�����û������������׳̶ȡ���������������ˮ�������ǿ����
��2�������Ը��ݽ���������ԭ��ص缫ʱʧ�������׳̶�ȷ�������Ļ����ԣ�
��� �⣺I����1��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��ǿ���ܺ������η�Ӧ�������ᣬ�������������Ϊ��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��
�ʴ�Ϊ��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ��
��2����ϡ�����̼���Ʒ�Ӧ��ȡ������̼���ö�����̼��ˮ��������Һ��Ӧ��ȡ���ᣬ����A��Һ��Ϊϡ���ᡢB�й���Ϊ̼���ơ�C����ҺΪ��������Һ��
�ʴ�Ϊ��ϡ���̼���ƣ���������Һ��
��3���ձ�C�з�����Ӧ�����ӷ���ʽΪ������̼��ˮ��������ӷ�Ӧ����̼������Ӻ��ᣬ���ӷ���ʽΪCO2+H2O+SiO32-=H2SiO3��+CO32-��
�ʴ�Ϊ��CO2+H2O+SiO32-=H2SiO3��+CO32-��
��4��ϡ�����̼���Ʒ�Ӧ���ɶ�����̼��ˮ��������̼��ˮ�����Ʒ�Ӧ���ɹ��ᣬ����ǿ����ȡ����֪������ǿ��˳�����̼����ᣬ��ǽ�����S��C��Si��
�ʴ�Ϊ��S��C��Si��
II����1��C��������������Һ��Ӧ���ɵ���������C����Һ�����ǣ��ʴ�Ϊ����Һ����ǣ�
��2�������������ӷ�Ӧ����������������ӣ��䷴Ӧ�����ӷ���ʽΪ��Cl2+S2-=2Cl-+S�����ʴ�Ϊ��Cl2+S2-=2Cl-+S����
��3�������ж�������Ⱦ����������Ҫ����β���������ʴ�Ϊ��û�н���β��������
III����1��A����Ƭ��������ͭ��Һ����ͭ������Fe�Ļ����Դ���Cu��˵��Fe�Ľ����Դ���Cu����A��ȷ��
B����������ǿ�����ԣ��ܽ���۽������������̬������ͭ��������Ӧ�ֱ�����FeCl3��CuCl2��˵����������ǿ�����ԣ�������֤��Fe��Cu�Ľ�����ǿ������B����
C��ͭƬ����FeCl3��Һ�У�ͭƬ���ܽ⣺2FeCl3+Cu=2FeCl2+CuCl2��˵����ԭ����ͭ����ǿ���������ӣ�����˵�����Ľ����Ա�ͭǿ����C����
D����Ƭ��ͭƬ�ֱ�����ʢ��ϡ������ձ��У���Ƭ�������ݲ�������ͭƬ�����ݣ�˵�����Ļ����Դ���Cu����Fe�Ľ����Դ���Cu����D��ȷ��
E�������£�Fe��Ũ���ᷢ���ۻ�����ͭ�ܺ�Ũ���ᷢ��������ԭ��Ӧ������˵��Fe�Ľ����Դ���Cu����E����
��ѡAD��
��2���ٸ��ݽ���������ԭ��ص缫ʱʧ�������׳̶�ȷ�������Ļ����ԣ���Fe��Cu���õ�������ƽ�в���ϡ�����У�Fe�����ܽ⣬Cu�������������ɣ�������ӦFe+2H+=Fe 2++H2��������ʵ������֪��Fe�Ľ����Դ���Cu��
��װ��ͼΪ ��
��
�ʴ�Ϊ�� ��
��
��Fe��Cu���õ�������ƽ�в���ϡ�����У�����ԭ��أ�Feʧ������������Fe�����ܽ⣬Cu��������Cu�������������ɣ�
�ʴ�Ϊ��Fe�����ܽ⣬Cu�������������ɣ�
���� ���⿼���˷ǽ����ԵıȽϡ�����������ǿ�����жϣ������ڿ���ѧ����ʵ��̽�������ͶԻ���֪ʶ�ķ���Ӧ����������Ŀ�Ѷ��еȣ�ע�����Ԫ�������ɡ�����֮����û���Ӧ�ȶ�����ȷ�������Ľ�����ǿ����


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ���� | ||
| C�� | ���Ը��������Һ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1-��ϩ | B�� | 1��3-���ױ� | ||
| C�� | �ױ� | D�� | 2-��-3-�һ�-2-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬ�¶��£�0.6mol/L��ˮ��Һ��0.3mol/L��ˮ��Һ��c��OH-��֮����2��1 | |
| B�� | ��ϡ��ˮ��μ���ϡ�����У�����Һ��pH=7ʱ��c��SO42-����c��NH4+�� | |
| C�� | 25��ʱ��10mL 0.02mol•L-1HCl��Һ��10mL0.02mol•L-1Ba��OH��2��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ20mL������Һ��pH=12 | |
| D�� | 25��ʱpH=10��NaOH��Һ��60��ʱpH=10��NaClO��Һ�У�c��H+����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �٢ڢݢߢ� | C�� | �٢ڢ� | D�� | �٢ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��Mg��Al��ԭ�����μ��� | B�� | I2��Br2��Cl2������������ǿ | ||
| C�� | C��N��Oԭ�Ӱ뾶�������� | D�� | P��S��Cl��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��g��+$\frac{1}{2}$O2 ��g���TCO2��g����H=-283 kJ/mol | |
| B�� | CH4��g��+2O2��g���TCO2��g��+2H2O ��g����H=-802.3 kJ/mol | |
| C�� | 2H2��g��+O2��g���T2H2O ��l����H=-571.6 kJ/mol | |
| D�� | H2 ��g��+Cl2 ��g���T2HCl ��g����H=-184.6 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ���ᣨ2-�ǻ����ᣩΪ��ɫҺ�壬��ˮ���ܣ����ӷ��ԣ����ڶ������ﻯѧ��
���ᣨ2-�ǻ����ᣩΪ��ɫҺ�壬��ˮ���ܣ����ӷ��ԣ����ڶ������ﻯѧ��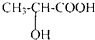
| ���� | 1 | 2 | 3 | 4 |
| ������mL�� | 19.22 | 19.18 | 19.80 | 19.20 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com