
关于如图所示装置的叙述,正确的是( )

A. 铜是阳极,铜片上有气泡产生
B. 盐桥中的阳离子会移向CuSO4溶液
C. 正极附近的SO42﹣离子浓度逐渐增大
D. 锌离子在锌片表面被还原
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: A.依据电极材料判断电极名称,正极发生还原反应,负极发生氧化反应;
B.阳离子带正电应移向原电池的正极;
C.原电池中,阴离子带负电应该移向原电池的负极;
D.依据原电池电极判断发生反应.
解答: 解:A.锌活泼性强于铜,做原电池负极,铜电极做正极,氢离子在铜电极上得到电子发生还原反应析出,故A错误;
B.阳离子带正电应移向原电池的正极,所以会移向铜电极附近,故B正确;
C.SO42﹣离子带负电,依据异性电荷相吸原理,应该移向负极,故C错误;
D.图中原电池,锌做负极,发生氧化反应,锌失去电子生成锌离子,故D错误;
故选:B.
点评: 本题考查了原电池工作原理,熟悉原电池工作原理、准确判断原电池的电极是解题关键,注意原电池中离子移动方向,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
已知某溶液Cl-、Br-、I-的离子数之比为1:2:3,要使溶液Cl-、Br-、I-的离子数之比变为3:2:1,则通入Cl2的分子数与原溶液中 I- 离子数之比为 ( )
A.1:2 B.1:3 C.2:1 D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列叙述正确的是( )
A.T、Q的氢化物常态下均为无色气体
B.L、M的单质与稀盐酸反应速率:M > L
C.R的氧化物对应的水化物可能具有两性
D.L、Q形成的简单离子核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某种一元强碱MOH溶液加入一种一元酸HA反应后,溶液呈中性,下列判断一定正确的是( )
A.加入的酸过量
B.生成的盐不水解
C.酸和碱等物质的量混合
D.反应后溶液中[A-]=[M+]
查看答案和解析>>
科目:高中化学 来源: 题型:
某二元酸(化学式用H2A表示)在水溶液中的电离方程式是H2A===H++HA-;HA-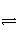

H++A2-。
回答下列问题:
(1)Na2A溶液显________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)________________________________________________________________________。
(2)若0.1 mol·L-1 NaHA溶液的pH=2,则0.1 mol·L-1 H2A溶液中氢离子的物质的量浓度可能__________0.11 mol·L-1(填“>”、“=”或“<”),理由是
________________________________________________________________________
__________________。
(3)0.1 mol·L-1 NaHA的溶液中各种离子浓度由大到小的顺序是
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
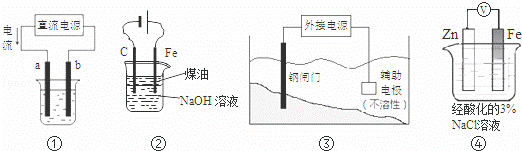
关于下列各装置图的叙述中,不正确的是( )
|
| A. | 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
|
| B. | 用图②装置实验室制备白色Fe(OH)2 |
|
| C. | 装置③中钢闸门应与外接电源的正极相连 |
|
| D. | 装置④中电子由Zn流向Fe,Zn极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,不正确的是( )
|
| A. | a mol/L的HCN溶液与b mol/L的NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN﹣),则a一定小于b |
|
| B. | 常温,CH3COONa溶液的pH=8,则c(Na+)﹣c(CH3COO﹣)=9.9×10﹣7mol/L |
|
| C. | 常温下,0.1mol/L的某酸溶液中,若c(OH﹣)/c(H+)=1×10﹣8,则溶液中由水电离出的c(H+)=1×10﹣11mol/L |
|
| D. | 在0.1mol/L的Na2SO3溶液中加入少量NaOH固体,c(SO32﹣)与c(Na+)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH,下列说法正确的是( )
A.浓度均为0.1 mol·L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
B.0.1 mol·L-1 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
C.NaF溶液中只含有Na+、F-、H+、OH-、H2O五种微粒
D.NaF溶液中加入少量NaOH固体,溶液中c(F-)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)2HBr(g) ΔH<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
A.a>b B.a=b
C.a<b D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com