
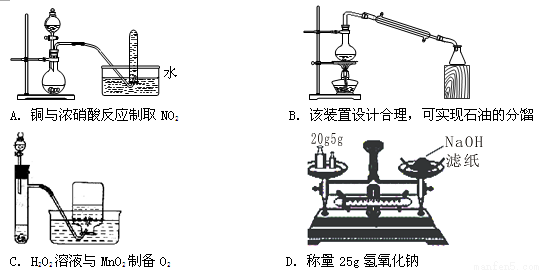
下列实验设计或实验操作中,正确的是
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期第三次月考理综试卷(解析版) 题型:填空题
选考[化学——选修3:物质结构与性质] (15分)
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu的第三能层的电子排布式 ,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有 (填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为 。
(2)PO43-的空间构型是 。
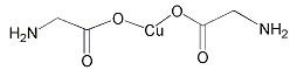
(3)氨基乙酸铜的分子结构如图,氮原子的杂化方式为 。
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则CN-中含有的σ键与π键的数目之比为 。
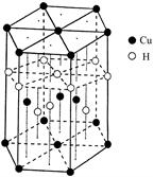
(5)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为 。
(6)铜晶体为面心立方最密堆积,铜的原子半径为r pm,则晶体铜密度的计算式为 g/cm3。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
A.2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l), △H2
B.H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2
C.C(s)+1/2O2(g)=CO(g),△H1; C(s)+O2(g)=CO2(g), △H2
D.S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g), △H2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol二氧化硅晶体中含有4NA个硅氧键
B.100mL 18.4mo1·L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA
C.0.1L 3mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3NA
D.将0.l mol FeC13滴入沸水中可制得0.1NA Fe(OH)3胶粒
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.二氧化碳结构式:O-C -O
B.S2-的结构示意图: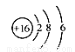
C.中子数为146、质子数为92的铀(U)原子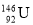
D.NH5的电子式为: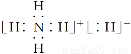
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:选择题
向一定量的Cu、Fe2O3的混合物中加人600mL 2mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,再加入过量1 mol/L NaOH溶液,将沉淀过滤、洗涤、干燥,称得质量比原混合物增重17.6g,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量是
A.4.8 g B.8.8 g C.9.6g D.14.4g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:填空题
(12分)铝及其化合物用途广泛。工业上焙烧明矾【KAl(SO4)2·12H2O】可得到A12O3,反应的化学方程式为4KAl(SO4)2·12H2O+3S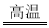 2K2SO4+2A12O3+9SO2↑+48H2O。
2K2SO4+2A12O3+9SO2↑+48H2O。
请回答下列问题:
(1)在焙烧明矾的反应中,被氧化和被还原的元素质量之比是________________。
(2)焙烧明矾时产生的SO2可用来制硫酸。已知25℃、10lkPa时:
①2SO2(g) +O2(g)  2SO3(g) ΔH=—197KJ/mol
2SO3(g) ΔH=—197KJ/mol
②2H2O(g)  2H2O(l)ΔH=—44KJ/mol
2H2O(l)ΔH=—44KJ/mol
③2SO2(g) +O2(g) + 2H2O(g) 2H2SO4(l)ΔH=—545KJ/mol
2H2SO4(l)ΔH=—545KJ/mol
则反应SO3(g)+ H2O(l)= H2SO4(l)ΔH=______KJ/mol。
(3)工业上利用电解熔融的A12O3制备Al,其化学方程式是_____________________;电解时阳极和阴极材料均为石墨,电解时所消耗的电极是__________(填“阳极”或“阴极”)。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式为____________;②电池总反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
A.Y的气态简单氢化物的热稳定性比W的强
B.X的最高价氧化物对应水化物的酸性比W的弱
C.Y分别与Z、W形成的化合物均为碱性氧化物
D.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com