
下列溶液与100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度相等的是( )
|
| A. | 200mL0.5mol/LNaCl溶液 | B. | 100mL1mol/LNa2CO3溶液 |
|
| C. | 100mL0.5mol/LNa3PO4溶液 | D. | 1L1mol/LNaOH溶液 |
考点:
物质的量浓度的相关计算.
分析:
电解质溶液中离子浓度=电解质浓度×化学式中相应离子数目,与溶液体积无关,100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度为1mol/L,结合选项计算判断.
解答:
解:100mL0.5mol/LNa2SO4溶液中 Na+的物质的量浓度0.5mol/L×2=1mol/L,
A.200mL0.5mol/LNaCl溶液中 Na+的物质的量浓度0.5mol/L×1=0.5mol/L,故A不符合;
B.100mL1mol/LNa2CO3溶液中 Na+的物质的量浓度1mol/L×2=2mol/L,故B不符合;
C.100mL0.5mol/LNa3PO4溶液中 Na+的物质的量浓度0.5mol/L×3=1.5mol/L,故C不符合;
D.1L1mol/LNaOH溶液中 Na+的物质的量浓度1mol/L×1=1mol/L,故D符合;
故选D.
点评:
本题考查物质的量浓度有关计算,比较基础,有利于基础知识的巩固.


科目:高中化学 来源: 题型:
在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)═2CO2(g)△H=﹣566kJ•mol﹣1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1
由1mol CO(g)和3mol CH4(g)组成的混合气体在上述条件下充分燃烧,恢复至室温释放的热量为( )
|
| A. | 2912kJ | B. | 2953kJ | C. | 3236kJ | D. | 3867kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
50mL0.001mol/L盐酸的pH=
50mL0.001mol/LNaOH溶液的pH=
100℃时,水的Kw=1×10﹣12,则该温度下,纯水的pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的△H前者大于后者的是( )
①C(s)+O2(g)═CO2(g);△H1 C(s)+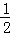 O2(g)═CO(g);△H2
O2(g)═CO(g);△H2
②S(s)+O2(g)═SO2(g);△H3 S(g)+O2(g)═SO2(g);△H4
③H2(g)+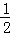 O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8.
|
| A. | ① | B. | ④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种含氨和氯化铵物质的量相等的混合溶液,其pH为9.3,下列说法中错误的是( )
|
| A. | 氨水的电离作用大于氯化铵的水解作用 |
|
| B. | 氯化铵的水解作用大于氨水的电离作用 |
|
| C. | 氨水的存在抑制了氯化铵的水解 |
|
| D. | 氯化铵的存在抑制了氨水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用CO生产甲醇的反应为CO(g)+2H2(g)⇌CH3OH(g).图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图.下列叙述错误的是( )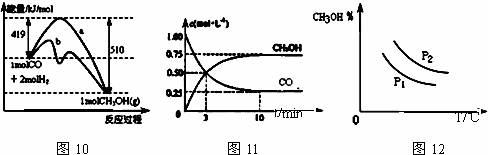
|
| A. | CO和H2合成CH3OH的反应:△H<0,△S>0 |
|
| B. | 保持温度不变,再充入1mol CO和2mol H2,反应达到新平衡时 |
|
| C. | 图10中曲线b可表示使用了催化剂的能量变化情况 |
|
| D. | 图12中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:
摩尔浓度相同的三种盐NaX、NaY和NaZ的溶液,其中pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
|
| A. | HX、HZ、HY | B. | HZ、HY、HX | C. | HX、HY、HZ | D. | HY、HZ、HX |
查看答案和解析>>
科目:高中化学 来源: 题型:
六氟化硫(SF6)具有良好的高压绝缘性,在电器工业中有着广泛的用途,SF6分子呈正八面体结构,S 原子位于正八面体的中心。下列关于SF6的推测中,正确的是
A.SF6在氧气中燃烧可生成SO2
B.SF6晶体是原子晶体
C.SF6是非极性分子
D.SF6中各原子的最外电子层都达到8电子稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com