
比较等物质的量浓度的:①H2SO3;②NaHSO3;③Na2SO3。三种溶液中[SO32-]的大小,排列正确的是( )
A.①>②>③ B.③>②>①
C.②>①>③ D.③>①>②
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
已知下列三个热化学方程式
①H2(g)+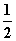 O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=131 kJ·mol-1
写出碳燃烧生成CO和CO燃烧的热化学方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)====CO(g)+3H2(g) ΔH=206.2 kJ·mol-1
CH4(g)+CO2(g)====2CO(g)+2H2(g) ΔH=247.4 kJ·mol-1
2H2S(g)====2H2(g)+S2(g) ΔH=169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例的空气,使部分H2S燃烧,其目的是___________________________ _______________________________;
_______________________________;
燃烧生成的SO2与H2S进一步反应,生成物在常温下均不是气体,写出该反应的化学方程式:_______________________________________。
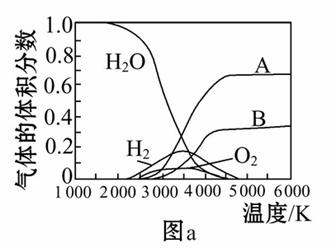
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图a所示。图中A、B表示的物质依次是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)  3C(g),已知加入1 mol A和3 mol B且达到平衡后,生成了a mol C。
3C(g),已知加入1 mol A和3 mol B且达到平衡后,生成了a mol C。
(1)达到平衡时,C在反应混合气中的体积分数是__________(用含字母a的代数式表示)。
(2)在相同实验条件下,若在同一容器中改为加入2 mol A和6 mol B,达到平衡后,C的物质的量为_______mol(用含字母a的代数式表示),此时C在反应混合气中的体积分数与原平衡相比___________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项中可说明HAc是弱电解质的是( )
A.0.1 mol·L-1HAc的pH>1
B.相同温度下,醋酸与强酸溶液的导电性比较
C.相同物质的量浓度、相同体积的醋酸和盐酸分别与足量的活泼金属反应时,消耗金属的量
D.pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液的酸碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
pH相同的盐酸溶液与醋酸溶液分别和锌粒反应,若最后锌都已完全溶解,放出的气体一样多,下列说法正确的是( )
A.反应所需时间:醋酸>盐酸
B.整个反应阶段的平均反应速率:醋酸>盐酸
C.开始的反应速率:盐酸>醋酸
D.参加反应的锌的质量:盐酸=醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下取0.2 mol·L-1的盐酸与0.2 mol·L-1的MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6。试回答下列问题:
(1)混合溶液中由水电离出的[H+]____ (填“>”“<”或“=”)0.2 mol·L-1盐 酸中水电离出的[H+]。
酸中水电离出的[H+]。
(2)求混合溶液中下列计算式的精确结果:
[Cl-]-[M+]=_________mol·L-1,[H+]-[MOH]=_________mol·L-1(填具体数字)。
(3)若室温下取0.2 mol·L-1的MOH溶液与0.1 mol·L-1的盐酸等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度__________ (填“>”“<”或“=”)MCl的水解程度,溶液中各离子浓度由大到小的顺序为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1 mol某纯物质的热效应,单位常用kJ·mol-1表示。已知在25℃的条件下:
Ag2O(s)+2HCl(g)===2AgCl(s)+H2O(l) ΔH1=-324.4 kJ·mol-1
2Ag(s)+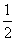 O2(g)===Ag2O(s) ΔH2=-30.56 kJ·mol-1
O2(g)===Ag2O(s) ΔH2=-30.56 kJ·mol-1
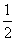 H2(g)+
H2(g)+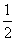 Cl2(g)===HCl(g) ΔH3=-92.21 kJ·mol-1
Cl2(g)===HCl(g) ΔH3=-92.21 kJ·mol-1
H2(g)+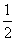 O2(g)===H2O(l) ΔH4=-285.6 kJ·mol-1
O2(g)===H2O(l) ΔH4=-285.6 kJ·mol-1
则25℃时氯化银的标准生成热为( )
A.-126.89 kJ·mol-1 B.-324.4 kJ·mol-1
C.-30.56 kJ·mol-1 D.题中数据不足,无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氧化还原反应的判断中正确的是( )
|
| A. | 金属单质与盐溶液不一定发生置换反应 |
|
| B. | 侯氏制碱法的原理属于氧化还原反应 |
|
| C. | 阳离子只有氧化性,阴离子只有还原性 |
|
| D. | 失电子的数目越多,说明该物质的还原性越强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com