
| A. | 进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | |
| B. | HCl溶液的酸性比H2S溶液的酸性强,则氯元素的非金属性比硫强 | |
| C. | H2O的沸点高于H2S,则氧元素的非金属性强于硫元素 | |
| D. | 浓H2SO4的氧化性强于HClO4,可确定硫和氯两种元素的非金属性强弱 |
分析 A、氢化物越稳定,对应元素的非金属性越强;
B、不能根据氢化物的酸性强弱来判断非金属性;
C、水分子间存在氢键;
D、最高价含氧酸的氧化性与元素的非金属性无必然关系.
解答 解:A.氢化物越稳定,对应元素的非金属性越强,则进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱,故A正确;
B.氢化物的酸性强,元素的非金属性不一定强,如HCl的酸性比HF强,但是非金属性:F>Cl,故B错误;
C、水分子间存在氢键,导致H2O的沸点高于H2S,与氧元素和硫元素的非金属性强弱无关,故C错误;
D、最高价含氧酸的氧化性与元素的非金属性无必然关系,应通过比较最高价含氧酸的酸性强弱来比较非金属性的强弱,故D错误.
故选A.
点评 本题考查非金属性的比较,题目难度不大,注意比较非金属性的角度,把握元素的性质与元素对应单质、化合物性质之间的关系.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:| 物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
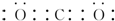
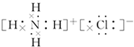

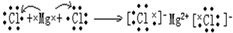 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ K+ HCO3- Cl- | B. | NH4+ Mg2+ SO32- Cl- | ||
| C. | K+ Na+ SO42- Cl- | D. | K+ Cu2+ CO32- NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中c(OH-)=0.1 mol/L,则BA(盐)溶液pH<7 | |
| B. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 | |
| C. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c (Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 4种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小顺序是②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓硝酸与蛋白质的颜色反应鉴别部分蛋白质 | |
| B. | 用分液漏斗从石油里分离出汽油、煤油和石蜡 | |
| C. | 可用水鉴别苯、四氯化碳、乙醇三种无色液体 | |
| D. | 用灼烧闻气味的方法可区别纯棉织物和纯毛织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的颜色不再变化 | |
| B. | 温度和体积一定时,容器内压强不再变化 | |
| C. | 1molH-H键生成的同时有2molH-I键断裂 | |
| D. | 各物质的物质的量浓度之比为2:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向海带灰浸取液中滴加硫酸、过氧化氢和淀粉后,溶液变蓝,说明海带中含碘 | |
| B. | 向浓缩海水中通入氯气,再吹入空气,可以将溴从海水中提取出来 | |
| C. | 埋入地下的铁制管道用连接镁的方法加以防护 | |
| D. | 石油的分馏和煤的干馏都属于化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com