
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
| A.SO2、H2S、Cl2 | B.SO2、O2、NH3 |
| C.SO2、CO2、O2 | D.HCl、H2S、HI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
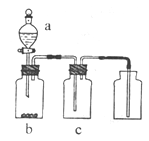
| | 气体 | a | b | C |
| A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
| B | SO2 | 浓硫酸 | 铜片 | 酸性KMnO4溶液 |
| C | CO2 | 稀硫酸 | Na2CO3固体 | 浓硫酸 |
| D | NH3 | 浓氨水 | 生石灰 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
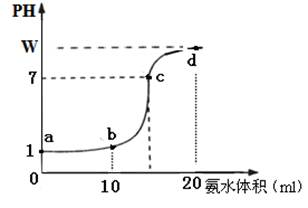
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验内容 | 实验现象 |
| A | 收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡。 | 蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色。 |
| B | 取出瓶内部分溶液,滴入紫色石蕊试液中直至过量。 | 紫色石蕊试液先变红色,后红色褪色。 |
| C | 取出瓶内剩下的部分溶液,滴入硝酸银溶液中。 | 产生大量白色沉淀 |
| D | 最后向瓶内倒入少量浓氢氧化钠溶液,振荡。 | 瓶内黄绿色气体立即消失。 |
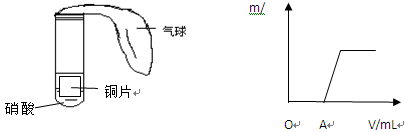
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
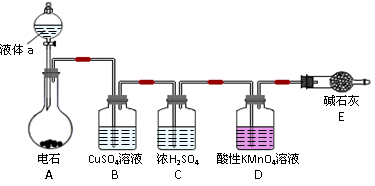
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
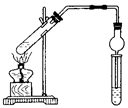
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
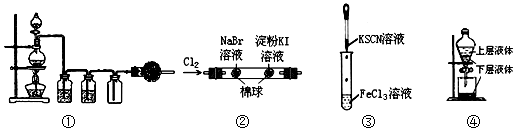
| A.①可用于实验室用MnO2固体与浓盐酸共热,制取并收集干燥、纯净的Cl2 |
| B.②实验中若左边棉花变橙色,右边棉花变蓝色,则能证明氧化性:Cl2>Br2>I2 |
| C.③实验试管中会生成血红色沉淀 |
| D.用图④操作可提取碘水中的碘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com