
| A. | 原混合气体中O2和CH4的体积比为2:1 | |
| B. | 残留物中只有Na2CO3 | |
| C. | 原混合气体中O2和CH4的物质的量之比为1:2 | |
| D. | 残留物只有Na2CO3和NaOH |
分析 将含有O2和CH4的混合气体置于盛有23.4g Na2O2的密闭容器中,电火花点燃反应为,CH4+2O2=CO2+2H2O;
2CO2+2Na2O2=2Na2CO3+O2;2H2O+2Na2O2=4NaOH+O2;根据题意可知反应结束后,容器内的压强为零(150℃),说明无气体剩余,则甲烷、氧气、过氧化钠全部反应,将残留物溶于水中,无气体产生说明无过氧化钠剩余,则23.4g Na2O2全部反应,物质的量为0.3mol;根据上述三个反应得到:2CH4+O2+6Na2O2=2Na2CO3+8NaOH;
解答 解:A、根据上述分析得到的反应可知,O2和CH4按照1:2恰好与0.3mol过氧化钠反应,无气体剩余,原混合气体中O2和CH4的体积比为2:1时,剩余甲烷,故A错误;
B、甲烷燃烧生成的气体有二氧化碳和水蒸气,所以和过氧化钠反应时残留物有Na2CO3和NaOH,故B错误;
C、根据上述分析得到的反应可知,O2和CH4按照1:2恰好与0.3mol过氧化钠反应,故C正确;
D、由题意结合分析得到的反应关系可知,残留物只有Na2CO3和NaOH,故D正确;
故选CD.
点评 本题考查了甲烷的性质、过氧化钠的性质、气体吸收后的产物判断和计算.


科目:高中化学 来源: 题型:选择题
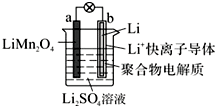
| A. | 充电时,a为阴极 | |
| B. | 充电时,溶液中Li+从b向a迁移 | |
| C. | 电池放电时负极反应为Li-e-═Li+ | |
| D. | 利用该电池电解水,消耗锂14 g可生成气体33.6 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D2、T2、H2互为同素异形体 | B. | 石墨、金刚石互为同位素 | ||
| C. | 甲烷和异丁烷互为同系物 | D. | 乙烷和乙烯互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 | 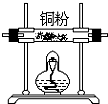 | 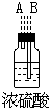 | 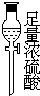 | 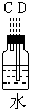 | 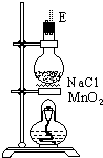 | 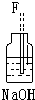 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com