
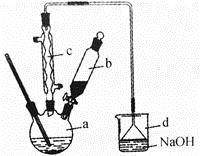
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| 苯 | 溴 | 溴苯 |
密度/g﹒cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须要做的是 (填入正确操作前的字母)
A.重结晶 B.过滤 C.蒸馏 D.萃取
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:2016-2017学年海南省高二上期中理化学试卷(解析版) 题型:填空题
氨在工农业生产中应用广泛。
(1)根 据下图写出合成氨的热化学方程式是________________________。
据下图写出合成氨的热化学方程式是________________________。
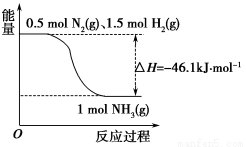
(2)将1 mol N2(g)和3 mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___________(填“大于”、“等于”或“小于”)92.2 kJ,原因是______________;若加入催化剂,ΔH________(填“变大”、“不变”或“变小”)。
(3)已知分别破坏1 mol N≡N键、1 mol H-H键时需要吸收的能量为946 kJ、4 36 kJ,则破坏1 mol N—H键需要吸收的能量为________kJ。
36 kJ,则破坏1 mol N—H键需要吸收的能量为________kJ。
(4)N2H4可视为NH3分子中的H被-NH2取代的产物。发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)==2NO2(g) ΔH1=+67.7 kJ·mol-1
N2H4(g)+ O2(g)==N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1
O2(g)==N2(g)+2H2O(g) ΔH2=-534 kJ·mol-1
则1 mol N2H4与NO2完全反应的热化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上周考化学试卷(解析版) 题型:选择题
已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定正确的是( )
A. 原子半径:X>Y>Z>W
B. W的含氧酸的酸性比Z的含氧酸的酸性强
C. W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
D. 若W与X原子序数差为5,则形成化合物的化学式为X3W2
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上模拟三化学试卷(解析版) 题型:填空题
选修3——物质结构与性质
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素,相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是 ,离子化合物YX5的电子式是 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐),A晶体的晶胞为正方体(如图1)。
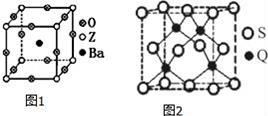
①制备A的化学反应方程式是 ;
②在A晶体中,Z的配位数为 ;
(4)R2+离子的外围电子层电子排布式为 。R2O的熔点比R2S的 (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B,B晶体的晶胞为正方体(如图2),若晶胞棱长为5.4×10-8cm,则晶胞密度为 g•cm﹣3(列式并计算)。
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上模拟三化学试卷(解析版) 题型:选择题
科学家们在研制一种吸气式的锂—空气电池,工作时吸收空气中的氧气在多孔金制成的正极表面上反应。总反应可表示为2Li+O2 Li2O2下列有关说法正确的是
Li2O2下列有关说法正确的是
A.充电时,多孔金制成的电极外接电源负极
B.放电时,Li+从负极向正极移动
C.放电时,吸收空气中22.4 L的O2,就有2 mol e-从电池负极流出
D.该电池可使用含Li+的水溶液作电解质溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是
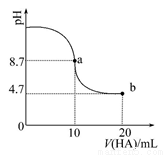
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相 同
同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列有关说法中正 确的是
确的是
A.1mol H2O2晶体中含有2molH+,但不自由移动
B.1mol羟基中含有的电子数为7NA
C.14g己烯和聚乙烯的混合物完全燃烧生成的CO2分子数为NA
D.标况下,22.4L溴乙烷中含有的共价键数为7 NA
NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二12月月考化学卷(解析版) 题型:推断题
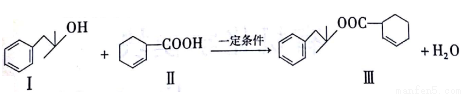
化合物III具有水果香味,在实验室可通过如下反应制得。
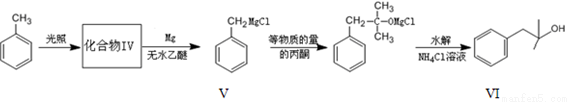
化合物I可通过下列路径合成:
(1)化合物III的分子式为___________________。
(2)化合物II能使Br2的 CCl4溶液褪色,该反应的化学方程式为________________。
(3)化合物IV的结构简式为___________,生成化合物IV的反应类型为______________。
(4)在浓硫酸和加热条件下,化合物I易发生消去反应生成含2个甲基的物质,该反应的化学方程式为____________________。
(5)写出满足下列条件化合物II的一种同分异构:______________。
①含有一个六元环 ②无酸性,酸性条件下水解生成两种有机物 ③ 能发生银镜反应
(6)CH3CH2MgBr和 也能发生类似V→VI的反应,请写出生成的醇的结构简式:_________________。
也能发生类似V→VI的反应,请写出生成的醇的结构简式:_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一12月月考化学卷(解析版) 题型:选择题
将一小块金属钠长期露置于空气中,最终的产物是
A.Na2CO3 B.Na2O C.NaOH D.Na2CO3·10H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com