
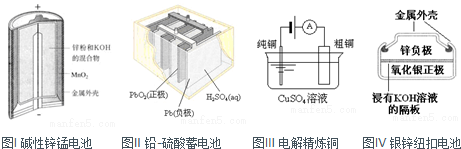
| A、图I所示电池中,的作用是催化剂 |
| B、图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C、图Ⅲ所示装置工作过程中,电解质溶液中浓度始终不变 |
| D、图IV所示电池中,是氧化剂,电池工作过程中还原为Ag |


科目:高中化学 来源: 题型:
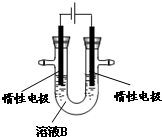
| A、生成的氢气中只含有H2 |
| B、生成的氢气中只含有D2 |
| C、生成的氢气中含有H2、HD、D2 |
| D、以上判断都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、臭氧是饮用水的理想消毒剂之一,因为它杀菌能力强且不影响水质 |
| B、因患“禽流感”而被捕杀的家禽尸体常用生石灰处理 |
| C、医疗上常用体积分数为75%的酒精进行皮肤消毒 |
| D、食品加工、消毒、防腐常使用福尔马林 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁在海水中比在河水中更易腐蚀,主要原因是海水含盐量高于河水 |
| B、NaFeO4自身处理水的原理与明矾和漂白粉共同处理水的原理相同 |
| C、高温或日常用的消毒剂可使H7N9型禽流感病毒蛋白质变性 |
| D、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br-、Fe2+、I- |
| B、Br-、I-、Fe2+ |
| C、I-、Fe2+、Br- |
| D、Fe2+、I-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
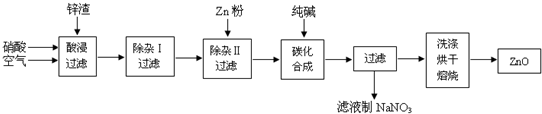
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com