
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
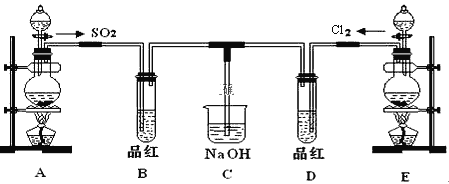
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:_______________________________;
(2)实验室用装置E制备Cl2,其反应的化学方程式为_______________________。除去Cl2中混有的HCl,可将气体通过盛有_______________________的洗气瓶。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:_________________________,D:________________________。
(4)停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________________________,D:__________________________。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)______________。
【答案】分液漏斗的玻璃塞没有取下来 MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O 饱和氯化钠的水溶液 品红褪色 品红褪色 褪色的品红又恢复成红色 无明显现象 Cl2+SO2+2H2O===2HCl+H2SO4
MnCl2+Cl2↑+2H2O 饱和氯化钠的水溶液 品红褪色 品红褪色 褪色的品红又恢复成红色 无明显现象 Cl2+SO2+2H2O===2HCl+H2SO4
【解析】
装置A生成的二氧化硫气体通过装置B中的品红溶液,二氧化硫具有漂白性,可以使溶液褪色,褪色后的溶液加热时又恢复原来的红色。氯气和水反应生成的次氯酸具有漂白性,因而氯气通入品红溶液中也能使品红褪色,次氯酸的漂白不可逆,加热时,不能恢复红色,剩余二氧化硫和氯气通过装置C吸收,防止污染空气,以此解答该题。
(1)塞子没有取下来,打开活塞时,空气无法进入分液漏斗内部,造成分液漏斗内的压强小于大气压强,液体无法流出,
故答案为:分液漏斗的玻璃塞没有取下来;
(2)实验室用二氧化锰和浓盐酸混合加热制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;除去Cl2中混有的HCl,可将气体通过盛有饱和氯化钠的水溶液
MnCl2+Cl2↑+2H2O;除去Cl2中混有的HCl,可将气体通过盛有饱和氯化钠的水溶液
的洗气瓶。
故答案为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;饱和氯化钠的水溶液;
MnCl2+Cl2↑+2H2O;饱和氯化钠的水溶液;
(3)SO2具有漂白性,二氧化硫通入品红溶液中,品红褪色;氯气和水反应生成的次氯酸具有漂白性,因而氯气通入品红溶液中也能使品红褪色;
故答案为:品红褪色;品红褪色;
(4)SO2的漂白具有可逆性,褪色后的溶液加热时又恢复原来的红色;次氯酸的漂白不可逆,加热时,不能恢复红色,
故答案为:褪色的品红又恢复成红色;无明显现象;
(5)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应:Cl2+SO2+2H2O===2HCl+H2SO4,生成物都无漂白性,因而SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不退色,
故答案为:Cl2+SO2+2H2O===2HCl+H2SO4。


科目:高中化学 来源: 题型:
【题目】已知下列数据:
物 质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
乙 醇 | -114 | 78.4 | 0.79 |
乙 酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.900 |
浓H2SO4 | 338 | 1.84 |



实验室制取乙酸乙酯的主要装置如上图I所示,主要步骤为:①在30mL的大试管中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到盛有10mL饱和Na2CO3溶液的(加入2滴酚酞试液)试管中;③小火加热试管中的混合液;④待小试管中收集约2mL产物时停止加热,撤出小试管并用力振荡,然后静置;⑤分离出纯净的乙酸乙酯。请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是_____________________________;
(2)写出该实验制取乙酸乙酯的化学方程式_________________________________,浓H2SO4的作用是 _______________________;
(3)步骤③中,用小火加热试管中的混合液,其原因_________________________;
(4)步骤④所观察到的现象是___________________________________________________
(5)步骤⑤中,分离出乙酸乙酯的方法是_________________________________;
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取圆底烧瓶中产物)。你认为哪种装置更合理,为什么?_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.氯化氢溶液能导电,所以氯化氢是电解质
C.固态氯化钾不导电,所以氯化钾是非电解质
D.液态硫酸不导电,所以硫酸是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A. 定容时仰视刻度线和液面
B. 容量瓶中原有少量的蒸馏水
C. 移液时,不慎将液体流到瓶外
D. 容量瓶盛过KOH溶液,使用前未洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S 和SO2 会对环境和人体健康带来极大的危害,工业上采取多种方法来减少这些有害气体的排放。
I.H2S 的除去
方法1: 生物脱H2S,反应的原理为H2S + Fe2(SO4)3==S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3 +2H2O。
2Fe2(SO4)3 +2H2O。
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105 倍,该菌的作用是______。
(2)由图1和图2 判断,使用硫杆菌的最佳条件为_________。若反应温度过高,反应速率下降,其原因是______________。


方法2: 在一定条件下,用H2O2 氧化H2S
(3)随着参加反应的n(H2O2)/n(H2S) 变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物 的分子式为________。
II.SO2 的除去
方法1( 双碱法): 用NaOH 吸收SO2 ,并用CaO 使NaOH 再生:NaOH 溶液![]() Na2SO3
Na2SO3
(4)写出过程①的离子方程式:_________________。
(5)CaO 在水中存在如下转化:CaO(s)+H2O(1)= Ca(OH)2(s)![]() Ca2+(aq) +2OH- (aq)。从平衡移动的角度,简述过程②NaOH再生的原理:_______________。
Ca2+(aq) +2OH- (aq)。从平衡移动的角度,简述过程②NaOH再生的原理:_______________。
方法2:用氨水除去SO2
(6)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol/L,溶液中的c(OH-)=________。将SO2 通入该氨水中,当c(OH-)降至1.0×10-7mol/L时,溶液中的c (SO32-)/c(HSO3-) =_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如图所示,下列有关说法正确的是( )

A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 该流程中得到晶体用到了溶解度的差异性
C. 流程图中的系列操作中用到的玻璃仪器可能有玻璃棒、烧杯、漏斗、坩埚等
D. 饱和食盐水中先通入的气体为CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏加德罗常数的说法正确的是
A. 1mol Na2O2与Na2O的固体混合物中,离子总数为3NA
B. 1mol Cl2与足量的NaOH溶液完全反应,转移电子的数目为2NA
C. 1mol/L的MgCl2溶液中含有的Cl-总数为NA
D. 6.4gCu在含0.2molH2SO4的浓硫酸溶液中加热充分反应,生成SO2气体的分子数总数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)查阅资料得酸性大小:H2CO3>苯酚>HCO3-。若用如图装置(部分夹持仪器省略)进行探究碳酸和苯酚的酸性强弱实验,下列叙述不正确的是( )
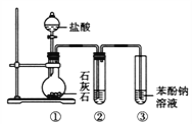
A. ②中试剂为饱和NaHCO3溶液
B. 打开分液漏斗旋塞,①产生无色气泡,③出现白色浑浊
C. 苯酚有弱酸性,是由于苯基影响了与其相连的羟基的活性
D. ③中发生反应的化学方程式是2![]() +CO2 +H2O→
+CO2 +H2O→![]() +Na2CO3
+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。其中反应④的离子方程式为 4 NH4++5O2=2 NO2-+6H++N2O+5H2O,下列说法正确的是
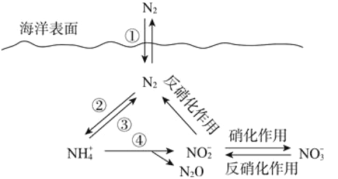
A. ①②均属于固氮反应
B. 海洋中的反硝化作用一定有氧气参加
C. 反应④中每生成 1molH2O 共转移 2mol e-
D. 向海洋排放含NO3- 的废水可能影响海洋中氮的循环
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com