
| A. | 1:10:100:1000 | B. | 1011:1010:10:1 | C. | 1:10:1010:1011 | D. | 14:13:2:3 |
分析 盐酸、氢氧化钠分别为一元强酸、一元强碱,溶液中氢离子浓度、氢氧根离子浓度分别等于其自身浓度,pH=-lgC(H+),根据溶液的pH计算溶液中氢离子浓度,根据氢氧化钠的浓度计算氢氧根离子浓度,再结合常温下,Kw=c(H+).c(OH-)10-14计算即可.
解答 解:①pH=1的醋酸溶液,pH=-lgC(H+)=1,C(H+)=0.1mol/L;
②盐酸为一元强酸,完全电离,0.01mol•L-1的盐酸,C(H+)=0.01mol/L;
③pH=11的氨水,pH=-lgC(H+)=11,则C(H+)=10-11 mol/L;
④氢氧化钠为一元强碱,完全电离,0.01mol•L-1的NaOH溶液,溶液中氢氧根离子浓度c(OH-)=0.01mol/L,Kw=c(H+).c(OH-)=c(H+)×0.01mol/L=10-14,解得c(H+)=1×10-12mol/L,
所以四种溶液中,H+浓度之比(①:②:③:④)=0.1mol/L:0.01mol/L:10-11 mol/L:1×10-12mol/L=1011:1010:10:1,
故选B.
点评 本题考查了pH的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键.


科目:高中化学 来源: 题型:选择题
| A. | Al3+、SO42-、NH3•H2O | B. | Na+、OH-、Cl2 | ||
| C. | K+、Ca2+、CO32- | D. | H+、Na+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
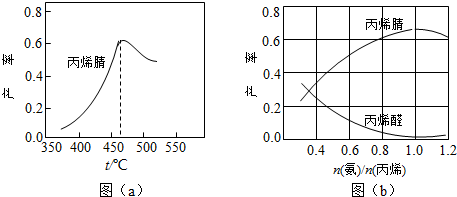
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
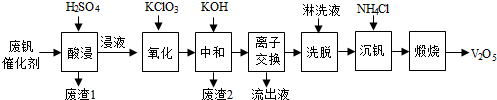
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中一定没有离子键,离子化合物中一定没有共价键 | |
| B. | 金属原子与非金属原子间一定以共价键相结合 | |
| C. | 由不同种原子形成的纯净物一定是化合物 | |
| D. | 石墨转化成全刚石要吸收热量,石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | n:(n+1) | C. | 1:(n+1) | D. | (n+1):n |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能够降低化学反应的反应热(△H) | |
| B. | 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关 | |
| C. | 原电池中发生的反应达平衡时,该电池仍有电流产生 | |
| D. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com