
| A. | 汽油与水互不相溶,可用裂化汽油萃取溴水中的溴 | |
| B. | 明矾能水解生成氢氧化铝胶体,可用作水的净化剂 | |
| C. | Na2CO3溶液具有碱性,可用热的浓Na2CO3溶液洗涤试管内壁的油污 | |
| D. | Mg(OH)2受热分解生成H2O和MgO且△H>0,可用Mg(OH)2作阻燃剂 |
分析 A、裂化汽油中含烯烃;
B、明矾水解成的氢氧化铝胶体对杂质有吸附作用;
C、油脂属于酯类,在碱性环境下会水解;
D、氢氧化镁受热分解为吸热反应,能吸收热量.
解答 解:A、裂化汽油中含烯烃,能和溴水发生加成反应,故不能用裂化汽油来萃取溴水中的溴,故A错误;
B、明矾水解成的氢氧化铝胶体对杂质有吸附作用,能起到净水的额作用,故明矾可以做净水剂,故B正确;
C、油脂属于酯类,在碱性环境下会水解,而碳酸钠是强碱弱酸盐,在水溶液中会水解显碱性,能导致油脂的水解从而起到去油污的作用,故C正确;
D、氢氧化镁受热分解为吸热反应,能吸收热量,从而可能使温度降低到低于可燃物的着火点,从而起到阻燃的作用,故D正确.
故选A.
点评 本题考查了化学知识在生活中的应用,难度不大,注意知识的积累.


科目:高中化学 来源: 题型:选择题
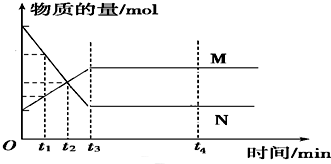
| A. | t1~t2时,只有正方向反应 | B. | t3~t4,反应不再发生 | ||
| C. | t3时,反应达到平衡 | D. | t3~t4,各物质的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池在放电时,Ag电极是电池的负极 | |
| B. | 充电时阳极发生的电极反应是:2Ag+2OH--2e-═Ag2O+H2O | |
| C. | 该电池可用酸作电解质溶液 | |
| D. | 充电时电流从Zn电极经电解质溶液流向外接电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
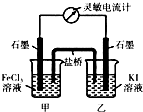
| 氯化铁溶液用量 | 10滴 | 20滴 | 30滴 | 2mL | 3mL | 4mL |
| 萃取后上层溶液颜色 | 黄色 | 黄色 | 黄色 | 较深黄色 | 黄色略带红色 | 黄红色 |
| 加入KSCN溶液后颜色 | 不变红 | 不变红 | 略变红 | 偏血红色 | 血红色 | 血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子立体构型 |
| A | SO2 | sp | 直线形 | 直线形 |
| B | HCHO | sp2 | 平面三角形 | 三角锥形 |
| C | NF3 | sp2 | 四面体形 | 平面三角形 |
| D | NH4+ | sp2 | 正四面体形 | 正四面体形 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
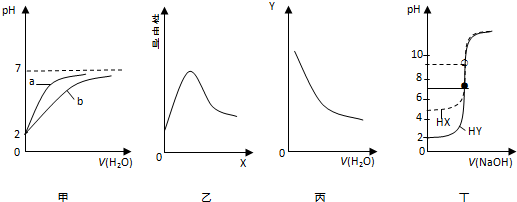
| A. | 图甲表示pH均为2的盐酸和醋酸分别用水稀释时pH变化曲线,其中a为醋酸 | |
| B. | 图乙表示0.1 mol•L-1 醋酸中加入X后溶液导电性曲线,则X可能是0.1 mol•L-1 氨水 | |
| C. | 图丙表示0.1 mol•L-1 氨水不断用水稀释曲线,Y可能是c(OH-) | |
| D. | 图丁表示0.0100 mol•L-1 NaOH溶液分别滴定20.00 mL 浓度均为0.0100 mol•L-1HX和HY的滴定曲线,可判断HX酸性比HY强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A | B | C | D |
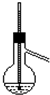 | 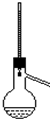 | 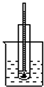 | 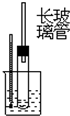 |
| A. | 酒精和浓硫酸混合加热制乙烯 | B. | 石油分馏实验 | ||
| C. | 苯跟溴的取代反应 | D. | 电石跟水反应制乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com