
| A.在平衡常数表达式中,反应物浓度用初始浓度,生成物浓度用平衡浓度 |
| B.在任何条件下,化学平衡常数是一个恒定值 |
| C.平衡常数的大小只与浓度有关,而与温度、压强、催化剂等无关 |
| D.从平衡常数的大小可以推断一个反应进行的程度 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题


| A.反应进行到3min时达到化学平衡状态 |
| B.是否使用催化剂对反应前后的能量变化没有影响 |
| C.当反应物消耗量一定时,若反应生成液态甲醇,能量变化值会更大 |
| D.平衡时氢气的浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+C(s),T=980 K时,ΔH-TΔS=0,当体系温度低于980 K时,估计ΔH-TΔS应__________0(填“大于”“小于”或“等于”),该反应________________进行;当体系温度高于980 K时,ΔH-TΔS应________________0。在冶金工业中,以碳作还原剂,温度高于980 K时的氧化产物以________________为主,低于980 K时以________________为主。
CO2(g)+C(s),T=980 K时,ΔH-TΔS=0,当体系温度低于980 K时,估计ΔH-TΔS应__________0(填“大于”“小于”或“等于”),该反应________________进行;当体系温度高于980 K时,ΔH-TΔS应________________0。在冶金工业中,以碳作还原剂,温度高于980 K时的氧化产物以________________为主,低于980 K时以________________为主。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。
2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间t变化如图曲线(Ⅰ)所示。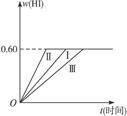
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AB(g)达到限度的标志是( )
2AB(g)达到限度的标志是( )| A.单位时间内生成n mol A2同时生成n mol AB |
| B.容器内的总物质的量不随时间变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.单位时间内生成n mol A2的同时生成n mol B2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.升高温度、降低压强、增加氮气 | B.降低温度、增大压强、加入催化剂 |
| C.升高温度、增大压强、增加氮气 | D.降低温度、增大压强、分离出部分氨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
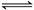 Z(g),达到平衡后生成a mol Z,下列说法错误的是
Z(g),达到平衡后生成a mol Z,下列说法错误的是| A.达到平衡时-v正(Y)=-v逆(Z) |
| B.若向平衡混合物中充入氦气,平衡向左移动 |
| C.若最初向容器中通入的是3molX和3molY,达平衡后Z的物质的量分数为 |
| D.若最初向容器中通入的是3molX、2molY、1molZ,达平衡后容器中n(Z)<3amol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
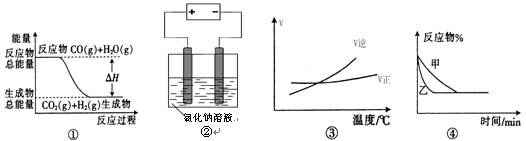


A.图①表示可逆反应“CO(g) + H2O(g) CO2(g)+H2(g)”中的ΔH大于0 CO2(g)+H2(g)”中的ΔH大于0  | B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1  | C.图③可表示可逆反应“A2(g)+3B2(g) 2AB3(g)”的ΔH小于0 2AB3(g)”的ΔH小于0  | D.图④可表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com