
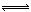 b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的
b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的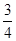 ,则a和b的数值可能是
,则a和b的数值可能是| A.a =1,b =1 | B.a =2,b =1 |
| C.a =2,b =2 | D.a =3,b =2 |
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.生成物的产量一定增大 | B.生成物的百分含量一定增大 |
| C.反应物的浓度一定降低 | D.每种反应物的转化率一定增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
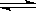 R(g) + S(g)。下列说法中可以充分说明这一反应已经达到化学平衡的是
R(g) + S(g)。下列说法中可以充分说明这一反应已经达到化学平衡的是| A.P、Q、R、S的浓度相等 |
| B.P、Q、R、S在密闭容器共存 |
| C.P、Q、R、S的浓度不再变化 |
| D.用P来表示的反应速率与用Q表示的反应速率相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2NO + O2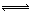 2NO2(放热) 2NO2(放热) | B.N2O4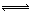 2NO2(吸热) 2NO2(吸热) |
C.Br2(g)+ H2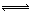 2HBr(放热) 2HBr(放热) | D.2NO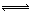 N2 + O2(吸热) N2 + O2(吸热) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
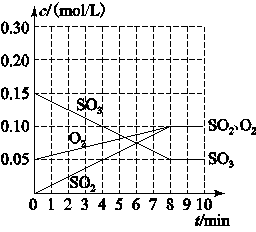
| | A | B | C | D |
| SO3 | 1 mol | 3 mol | 3 mol | 0 mol |
| SO2 | 2 mol | 1.5 mol | 0 mol | 6 mol |
| O2 | 2 mol | 1 mol | 0 mol | 5 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 z C(g),平衡时测得A的浓度为 0.5 mol/L,保持温度不变,将容器的容积压缩到原来的1/2,再达平衡时测得A的浓度为 0.8mol/L,下列判断正确的是( )
z C(g),平衡时测得A的浓度为 0.5 mol/L,保持温度不变,将容器的容积压缩到原来的1/2,再达平衡时测得A的浓度为 0.8mol/L,下列判断正确的是( )| A.x+y ﹤z | B.平衡向正反应方向移动 |
| C.B的物质的量增大 | D.C的体积分数保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
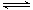 2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。
2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。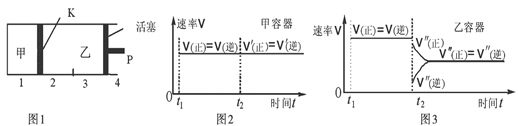
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持活塞位置不变,改变温度,达到新的平衡后,甲、乙中B的体积分数均增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g) + H2(g);△H=" -Q" kJ·mol-1(Q>0)。已知达到平衡时,CO为0.12mol。试回答:
CO(g) + H2(g);△H=" -Q" kJ·mol-1(Q>0)。已知达到平衡时,CO为0.12mol。试回答:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
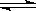 4NH3(g)+3O2(g) △H =" a" kJ.mol-1
4NH3(g)+3O2(g) △H =" a" kJ.mol-1| 温度T/K | 303 | 313 | 323 |
| NH3生成量/(10—6mol) | 4.8 | 5.9 | 6.0 |
 g)
g) 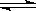 3NH3(g) △H =" —92.4" kJ.mol-1
3NH3(g) △H =" —92.4" kJ.mol-1 2N2(g) + 6H2O(l)
2N2(g) + 6H2O(l) 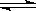 4NH3(g) + 3O2(g)△H = _________。(3分)
4NH3(g) + 3O2(g)△H = _________。(3分)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com