


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
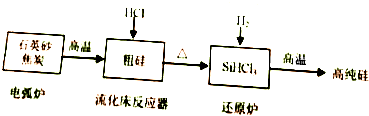 硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中有广泛应用,回答下列问题:
硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中有广泛应用,回答下列问题:| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| m-n | 0 | 1 | 2 | 3 |
| 含氧酸强度 | 弱 酸 | 中 强 | 强 | 很 强 |
| 实 例 | HClO | H3PO4 | HNO3 | HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学欲探究Cl2、Br2、I2之间的变化:
某同学欲探究Cl2、Br2、I2之间的变化:查看答案和解析>>
科目:高中化学 来源: 题型:
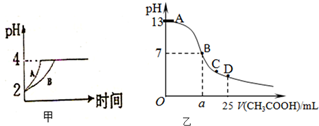 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.15 mol?L-1 |
| B、0.30 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、简单离子半径:Y>Z>W>Q>X |
| B、W2Z2与X2Z反应中氧化剂与还原剂物质的量之比为1:2 |
| C、X能分别与Y、Z、W形成共价化合物 |
| D、Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com