
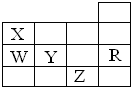
 如图为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )
如图为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |


查看答案和解析>>
科目:高中化学 来源: 题型:
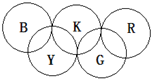 如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:
如图所示,形成奥运五环的B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系: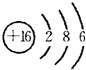



查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省红色六校高三第二次联考理综化学试卷(解析版) 题型:填空题
X、Y、Z、M、N、Q为元素周期表前四周期的六种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X元素在周期表中的位置是?????????????? ,属于????? 区元素,它的外围电子的电子排布图为??????????????????????????????? 。

(2)XZ2分子的立体结构是?????????????? ,YZ2分子中Y的杂化轨道类型为????????? ,相同条件下两者在水中的溶解度较大的是?????????????????????????? (写分子式),理由是????????????????????????????????????????????????????????????????????? 。
(3)含有元素N的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,其原因是 ?????? 。
(4)元素M与元素Q形成晶体结构如图所示,设其晶胞边长为a pm,则a位置与b位置之间的距离为_______pm(只要求列算式)。
查看答案和解析>>
科目:高中化学 来源:江苏月考题 题型:单选题
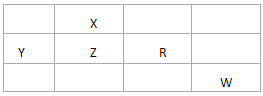
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com