
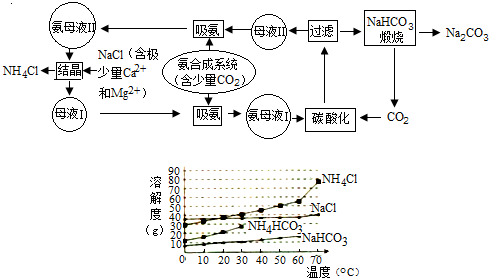
分析 以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,联合制碱法包括两个过程:第一个过程是将氨通入饱和食盐水而成氨盐水,再通入二氧化碳,发生反应:NH3+H2O+CO2=NH4HCO3.在溶液中就有了大量的钠离子、铵根离子、氯离子、碳酸氢根离子,这其中NaHCO3溶解度最小,所以析出,发生反应:NH4HCO3+NaCl=NH4Cl+NaHCO3↓.再利用碳酸氢钠不稳定性,受热容易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,得到纯碱,其滤液是含有氯化铵和氯化钠的溶液,第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用.
由流程图可知,母液Ⅰ由母液Ⅱ析出NH4Cl得到,故母液Ⅰ为NaCl溶液、母液Ⅱ为氯化铵和氯化钠的溶液.
解答 解:以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,联合制碱法包括两个过程:第一个过程是将氨通入饱和食盐水而成氨盐水,再通入二氧化碳,发生反应:NH3+H2O+CO2=NH4HCO3.在溶液中就有了大量的钠离子、铵根离子、氯离子、碳酸氢根离子,这其中NaHCO3溶解度最小,所以析出,发生反应:NH4HCO3+NaCl=NH4Cl+NaHCO3↓.再利用碳酸氢钠不稳定性,受热容易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,得到纯碱,其滤液是含有氯化铵和氯化钠的溶液,第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体.由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品.此时滤出氯化铵沉淀后所得的滤液,已基本上被氯化钠饱和,可回收循环使用.
(1)由流程图可知,母液Ⅰ由母液Ⅱ析出NH4Cl得到,由上述分析可知,母液Ⅰ的主要成分是NaCl,氨母液Ⅰ碳酸化时发生反应的化学方程式为:NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3↓,高于35℃NH4HCO3开始分解,氨母液Ⅰ保持在30℃~35℃下碳酸化,原因是:防止碳酸氢铵分解,
故答案为:NaCl;NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3↓;防止碳酸氢铵分解;
(2)在NaHCO3过滤后,将NH4Cl分离并使用剩余的母液回至制碱系统复用,是联碱法与氨碱法的主要区别,母液循环析出,除加入NaCl固体外,还应采取的措施是:通入氨气,
故答案为:通入氨气;
(3)从母液Ⅱ中析出的NH4Cl中可能含有NaCl,取少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化铵产品纯净,
故答案为:取少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化铵产品纯净.
点评 本题考查侯德邦制碱法,掌握原理是解题的关键,是对学生综合能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸的反应 | B. | Ba(OH)2.8H2O与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 稀盐酸与稀氢氧化钠溶液的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③④ | C. | ①②③④ | D. | 只有①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能是7 | B. | 只能是15 | C. | 是11或15 | D. | 是11或13 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
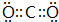 ,B与D形成的原子个数比为1:1的化合物的电子式是
,B与D形成的原子个数比为1:1的化合物的电子式是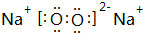 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H20
+H20| 相对分子质量 | 密度(g/cm3) | 沸点(℃) | 水中溶解性 | |
| 正丁酸 | 88 | 0.9587 | 163.5 | 溶 |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 丁酸异戊酯 | 158 | 0.886 | 179 | 不溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +NaCl+3H2O.
+NaCl+3H2O. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com