
| A. | 与水反应中既是氧化剂又是还原剂 | B. | 与NaOH反应生成溴化钠和次碘酸钠 | ||
| C. | 可作氧化剂 | D. | 与水反应是氧化还原反应 |
分析 IBr中I元素的化合价为+1价,Br为-1价,IBr化学性质与卤素单质具有相似性,及反应IBr+H2O═HBr+HIO中没有元素化合价的变化来分析解答.
解答 解:A.溴化碘与水作用时,该反应中没有电子转移,不属于氧化还原反应,故A错误;
B.IBr+H2O═HBr+HIO,生成的酸能和NaOH反应,所以溴化碘和NaOH反应生成NaIO、NaBr、H2O,故故B正确;
C.溴化碘的化学性质与卤素单质相似,则IBr中I元素的化合价为+1价,I元素的化合价在反应中能降低,则在很多化学反应中IBr是强氧化剂,故C正确;
D.反应中元素化合价没有发生变化,不是氧化还原反应,故D错误.
故选BC.
点评 本题考查了氧化还原反应,为高频考点,明确元素化合价是解本题关键,注意溴化碘中两种元素的化合价,再采用知识迁移的方法分析解答.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:解答题
 铁及其化合物是一类重要的物质,在人类的生产和生活中具有广泛的用途.
铁及其化合物是一类重要的物质,在人类的生产和生活中具有广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下1molO2与其他物质发生反应时转移的电子数一定为4NA | |
| B. | 1L 0.1 mol/L的Na2CO3溶液中,Na+、CO32-总数为0.3 NA | |
| C. | 28g C18O中含有的质子数为14 NA | |
| D. | 锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4L,锌失去电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2均为0.18mol/L | B. | N2为0.15mol/L | ||
| C. | N2为0.2mol/L,H2为0.6mol/L | D. | NH3为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
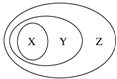 如表所列物质或概念间的从属关系符合如图所示关系的是( )
如表所列物质或概念间的从属关系符合如图所示关系的是( )| 选项 | X | Y | Z |
| A | 光导纤维 | 酸性氧化物 | 传统无机非金属材料 |
| B | 纯碱 | 碱 | 化合物 |
| C | 氧化物 | 化合物 | 纯净物 |
| D | H2SO4 | 含氧酸 | 强酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
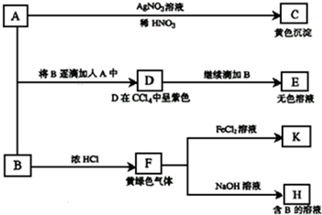
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
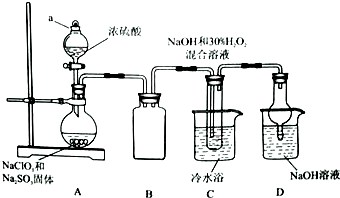 实验室欲制备高效漂白剂亚氯酸钠(NaCLO2),并对其样品进行分析.
实验室欲制备高效漂白剂亚氯酸钠(NaCLO2),并对其样品进行分析.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com