
| A.稳定性:HF > HCl > HBr > HI | B.碱性:NaOH > Mg(OH)2 > Al(OH)3 |
| C.酸性:H2SO4 > H3PO4 > HClO4 | D.氧化性:O2 > S > Se |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.微粒半径:S﹥S2―﹥Cl―﹥F | B.酸性:HClO4﹥H2SO4﹥H3PO4 |
| C.氧化性:Cl2﹥S﹥Se﹥Te | D.离子还原性:S2―﹥I―﹥Br―﹥OH― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用100mL的容量瓶准确量取100mL液体 |
| B.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 |
| C.用托盘天平称量NaCl时,NaCl放在纸上; 称量NaOH时,NaOH放在小烧杯里 |
| D.用加热的方法提取NH4C1固体中的少量碘单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
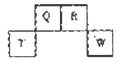
| A.非金属性:Q <W |
| B.Q、R、W三种元素的常见单质中所含微粒间的作用力完全相同 |
| C.原子半径:X>T;离子半径:X+<Y2- |
| D.T单质能与X的最高价氧化物的水化物反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.18O2和16O2是两种不同的核素 | B.甲醇(CH3OH)属于离子化合物 |
| C.N5和N2是氮元素的两种同位素 | D.由N5变成N2是化学变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Z+W
Z+W
 混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)
混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com