
һ�������£����ݻ�Ϊ10L���ܱ������У���l mol X��1 mol Y�������·�Ӧ��
2X(g)��Y(g) Z(g)����60 s�ﵽƽ������0.3mol��Z������˵����ȷ����
A��60 s��X��ƽ����Ӧ����Ϊ0.0005 mol��L-1��s-1
B�����¶Ⱥ�������䣬������������1 mol X��Y��ת���ʽ�����
C�����������ݻ���Ϊ20 L��Z����ƽ��Ũ�Ƚ�����ԭƽ��Ũ�ȵ�1/2
D���������¶ȣ�X�������������������Ӧ�ġ�H>0
B
����: 2X(g)��Y(g) Z(g)
��ʼ����mol�� 1 1 0
ת������mol�� 0.6 0.3 0.3
ƽ������mol�� 0.4 0.7 0.3
��60 s��X��ƽ����Ӧ����Ϊ![]() ��
��
�����¶Ⱥ�������䣬����X��Ũ�ȣ��������������Ӧ���ת���ʣ�������ת���ʻή�͡���Ϊ��Ӧ�������С�Ŀ��淴Ӧ�������������Ϊ20Lʱ����ϵ��ѹǿ���ͣ�ƽ�����淴Ӧ�����ƶ�������Z����ƽ��Ũ�Ƚ�С��ԭƽ��Ũ�ȵ�1/2�������¶ȣ�X�������������˵��ƽ�����淴Ӧ�����ƶ����������Ӧ�Ƿ��ȷ�Ӧ��������ȷ�Ĵ���B��


 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
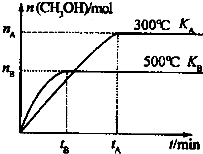 CO��H2�����ǵ�����������ȷ���������أ�
CO��H2�����ǵ�����������ȷ���������أ�| 1 |
| 2 |
| 1 |
| 2 |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��60 s��X��ƽ����Ӧ����Ϊ0.001 mol?L-1?s-1 | ||
B�����������ݻ���Ϊ20 L��Z����ƽ��Ũ�Ƚ�����ԭƽ��Ũ�ȵ�
| ||
| C�����¶Ⱥ�������䣬������������1 mol X��Y��ת���ʽ����� | ||
| D���������¶ȣ�X�������������������Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com