

分析 (1)①为蒸馏烧瓶,②为冷凝管;
(2)容量瓶、分液漏斗带有活塞或瓶塞,需要检查是否漏水;
(3)溴在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开,再用蒸馏的方法分馏得到四氯化碳;
(4)①配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到250mL容量瓶中(没有210mL容量瓶),并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀;
②实验室没有210mL的容量瓶,应配制250mL,根据溶液稀释前后溶质质量不变计算;
③分析操作对溶质物质的量、溶液体积的影响,结合c=$\frac{n}{V}$分析对溶液浓度的影响.
解答 解:(1)仪器①为蒸馏烧瓶,仪器②为冷凝管,
故答案为:蒸馏烧瓶;冷凝管;
(2)蒸馏烧瓶、冷凝管不需要检查是否漏水,因蒸馏装置,加热时产生气体,故需检查气密性,容量瓶、分液漏斗带有活塞或瓶塞,需要检查是否漏水,
故答案为:③④;
(3)溴在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开,再用蒸馏的方法分馏得到溴与四氯化碳,萃取剂应满足:常温下为液态、Br2在其中溶解程度大、与水互溶程度小、与Br2不反应,
故答案为:Ⅱ;萃取分液;Ⅰ;蒸馏;ACE;
(4)①配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到250mL容量瓶中(没有210mL容量瓶),并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀,
所以仪器除量筒、烧杯、玻璃棒、胶头滴管等外,还需要250mL容量瓶,图中没有提供250mL容量瓶,
故答案为:无;250mL容量瓶,
②实验室没有210mL的容量瓶,应配制250mL,设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变,则VmL×1.84g/cm3×98%=0.25L×0.18mol•L-1×98g/mol,解得V=2.4,
故答案为:2.4;
③A.用相同装置配制过0.10mol/L的硫酸溶液后,未清洗即进行此实验的配制,容器壁上会沾有硫酸,导致所配溶液浓度偏高,故选;
B.移液时未对烧杯和玻璃棒进行洗涤,移入容量瓶中的硫酸偏少,所配溶液浓度偏低,故不选;
C.定容时仰视刻度线,液面在刻度线上方,所配溶液体积偏大,导致溶液浓度偏低,故不选;
D.颠倒摇匀后发现液面低于刻度线,溶液残留在瓶塞与瓶口之间,但未加水至刻度线,不影响溶液浓度,故不选,
故选:A.
点评 本题考查物质的分离提纯、一定物质的量浓度溶液配制,属于拼合型题目,侧重对基础知识的巩固,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 乙烷 | B. | 丙烷 | C. | 正丁烷 | D. | 异戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽油是纯净物,乙醇汽油是混合物 | |
| B. | 塑料、橡胶、纤维是三种重要的有机高分子材料 | |
| C. | 变质的油脂有难闻的特殊气味,是因为油脂发生了加成反应 | |
| D. | 乙烯、植物油和苯都能与氢气发生加成反应,是因为其结构中都含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(B)=0.6 mol/(L•min) | B. | V(A)=0.3 mol/(L•min) | ||
| C. | V(B)=0.02/(L•S) | D. | V(C)=0.5 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

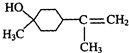 ;γ松油醇:
;γ松油醇: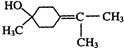 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动 | B. | x+y>z | ||
| C. | B的转化率提高 | D. | C的体积分数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、NO${\;}_{3}^{-}$、SCN-、CO${\;}_{3}^{2-}$ | B. | Fe2+、H+、Cl-、ClO- | ||
| C. | Mg2+、Na+、CH3COO-、SO${\;}_{4}^{2-}$ | D. | Na+、AlO${\;}_{2}^{-}$、Cl-、HCO${\;}_{3}^{-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com