


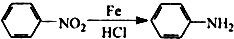 :苯胺中氨基易被氧化.
:苯胺中氨基易被氧化.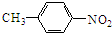 ,B为
,B为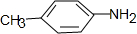 ,据反应①知C为
,据反应①知C为 ,C→D是氧化甲基成羧基,D→E是在苯环上引入Br原子,E为
,C→D是氧化甲基成羧基,D→E是在苯环上引入Br原子,E为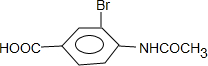 ,E→F是肽键水解成氨基,可见,B→C是为了保护氨基不被氧化;据已知反应①并结合Y的分子式可见,X→Y是羟醛缩合反应,Y的结构简式应为:
,E→F是肽键水解成氨基,可见,B→C是为了保护氨基不被氧化;据已知反应①并结合Y的分子式可见,X→Y是羟醛缩合反应,Y的结构简式应为: ,Z的结构简式为:
,Z的结构简式为: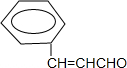 ,据此进行解答.
,据此进行解答. ,B为
,B为 ,据反应①知C为
,据反应①知C为 ,C→D是氧化甲基成羧基,D→E是在苯环上引入Br原子,E为
,C→D是氧化甲基成羧基,D→E是在苯环上引入Br原子,E为 ,E→F是肽键水解成氨基,可见,B→C是为了保护氨基不被氧化;据已知反应①并结合Y的分子式可见,X→Y是羟醛缩合反应,Y的结构简式应为:
,E→F是肽键水解成氨基,可见,B→C是为了保护氨基不被氧化;据已知反应①并结合Y的分子式可见,X→Y是羟醛缩合反应,Y的结构简式应为: ,Z的结构简式为:
,Z的结构简式为: ,
, ,故答案为:
,故答案为: ;
; ,C为
,C为 ,由B→C的反应方程式为:
,由B→C的反应方程式为: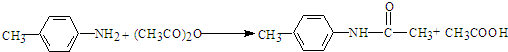 ,增加B→C反应的目的是保护易被氧化的氨基不被氧化,所以不能省略,
,增加B→C反应的目的是保护易被氧化的氨基不被氧化,所以不能省略,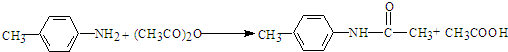 ;氨基易被氧化,在氧化反应之前需先保护氨基;
;氨基易被氧化,在氧化反应之前需先保护氨基; ,符合条件“①含有苯环结构、②与Z含有相同官能团”的Z的同分异构体中,若有两个取代基则有
,符合条件“①含有苯环结构、②与Z含有相同官能团”的Z的同分异构体中,若有两个取代基则有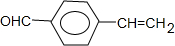 ,即其临位和间位共3种:
,即其临位和间位共3种: ,若只有一个取代基,则为
,若只有一个取代基,则为 ,
, 和
和 .
.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.20 | 24.00 |
| 第三次 | 10.00 | 0.40 | 21.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:6 | B、6:1 |
| C、1:5 | D、5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
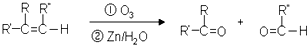

 到F反应是否进行完全,可用FeCl3溶液检验
到F反应是否进行完全,可用FeCl3溶液检验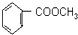 的最佳路线流程图(无机试剂任选).
的最佳路线流程图(无机试剂任选).| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了使一些肉制食品颜色更鲜红,可多加一些亚硝酸钠 |
| B、为了使婴儿对食品有浓厚兴趣,我们可以在婴儿食品中加少量着色剂 |
| C、食盐加碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿 |
| D、脂肪中必需脂肪酸的含量越高,其营养价值越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、食盐加碘,碘元素百分含量越高,食盐的质量越高 |
| B、菜炒熟出锅前再放碘盐以防分解,加醋会降低碘的利用率 |
| C、苯甲酸钠是常用的食品调味剂 |
| D、腌制肉食制品使用的亚硝酸盐即使不超标,也不可长期或大量的进食 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中滴入盐酸产生的气体能使澄清石灰水变浑浊,则溶液中含有CO32- |
| B、向某溶液中滴入KSCN溶液变为血红色,则溶液中一定含有Fe3+ |
| C、向某溶液中滴加硝酸酸化的BaCl2溶液,若产生白色沉淀,则溶液中一定含有SO42- |
| D、某溶液中通入CO2产生白色沉淀,则溶液中一定含有SiO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com