
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )。
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
用Pt作电极,电解100 mL 0.4 mol·L-1的NaCl溶液和100 mL 0.1 mol·L-1的稀硫酸,标准状况下产生0.224 L Cl2时停止电解,取出电极,将两烧杯溶液混合并冷却至常温,所得溶液的pH为(设气体产物全部逸出,混合溶液的总体积为200 mL)( )
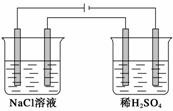
A.5 B.6 C.7 D.13
查看答案和解析>>
科目:高中化学 来源: 题型:
苹果酸的结构简式为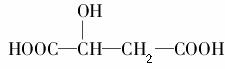 ,下列说法正确的是( )。
,下列说法正确的是( )。
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成1 mol H2
D.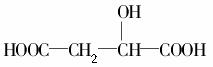 与苹果酸互为同分异构体
与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
向200 mL稀硝酸溶液中加入11.2 g铁粉,充分反应后,铁粉全部溶解并放出NO气体,溶液质量增加7.0 g,则所得溶液中Fe3+的物质的量浓度约为
( )。
A.0.1 mol/L B.0.2 mol/L
C.0.3 mo/L D.0.4 mo/L
查看答案和解析>>
科目:高中化学 来源: 题型:
我国目前制备多晶硅主要采用三氯氢硅氢还原法、硅烷热解法和四氯化硅氢还原法。由于三氯氢硅氢还原法具有一定优点,被广泛应用。其简化的工艺流程如下图所示:
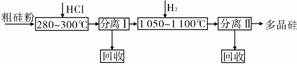
(1)由纯SiHCl3制备高纯硅的化学方程式为________________。该生产工艺中可以循环使用的物质是____________________(写出两种)。
(2)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法,工业上广泛采用的合成硅烷的方法是让硅化镁和固体氯化铵在液氨介质中反应得到硅烷,反应的化学方程式是______________________(不需注明反应条件,下同);整个制备过程必须严格控制无水,否则反应将不能生成硅烷,而是生成硅酸和氢气等,其化学方程式为_____________ _____;整个系统必须与空气隔绝,其原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组将一定质量的镁铝合金材料投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n(mol)与加入NaOH溶液的体积V(mL)的关系如图所示。
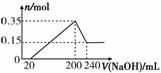
请回答下列问题:
(1)该合金材料中,镁、铝的物质的量之比为______。
(2)硫酸的物质的量浓度为______。
(3)另取相同质量的该合金材料与7.8 g Na2O2一起投入足量的H2O中,最终产生的气体在标准状况下的体积为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,生成N2和CO2。对此反应的下列叙述中正确的是( )
A.使用催化剂能加快反应的速率
B.使一种反应物过量能提高反应的速率
C.改变压强对反应速率没有影响
D.降低温度能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是( )
A.CO2和CH4都是引起“温室效应”的气体
B.Na2O、Na2O2的组成元素相同,故与CO2反应的产物也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.分别向新制氯水和久置氯水中滴加少量紫色石蕊试液,充分振荡后溶液都呈红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com