
| Cl2光照 |
| ① |
| NaOH溶液 |
| ② |
| Cu、O2、加热 |
| ③ |
| 银氨溶液加热、酸化 |
| ④ |
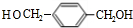 ,逆推可知B为
,逆推可知B为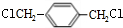 ,A为
,A为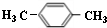 ,顺推可知D为
,顺推可知D为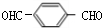 ,E为
,E为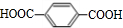 ,
,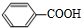 .
. ,逆推可知B为
,逆推可知B为 ,A为
,A为 ,顺推可知D为
,顺推可知D为 ,E为
,E为 ,
, ,上述反应中,反应①②属于取代反应,③④属于氧化反应,故答案为:
,上述反应中,反应①②属于取代反应,③④属于氧化反应,故答案为: ;①②;
;①②; +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl,
+2NaCl, +O2
+O2| Cu |
| △ |
 +2H2O,
+2H2O, +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl;
+2NaCl; +O2
+O2| Cu |
| △ |
 +2H2O;
+2H2O; )是合成纤维涤纶的一种单体,另一种单体是C(
)是合成纤维涤纶的一种单体,另一种单体是C( ),二者合成合成涤纶的化学方程式为:
),二者合成合成涤纶的化学方程式为: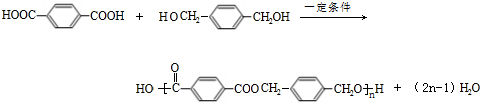 ,
, ;
; ,故答案为:
,故答案为: ;
;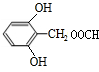 或
或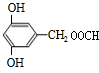 ,故答案为:
,故答案为: 或
或 .
.


科目:高中化学 来源: 题型:
| A、将氯化铵与草木灰混合施用 |
| B、纯碱既可以从内陆盐湖中提取,又可以用“侯氏制碱法”生产 |
| C、用石灰乳与硫酸铜溶液配制波尔多液 |
| D、高温煅烧石灰石可制生石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | a mol | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(NH4)2CO3 |
| B、NH4CNO |
| C、CH3COONH4 |
| D、NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com