
| A、碱性锌锰电池是二次电池 |
| B、MnO2发生了还原反应 |
| C、反应消耗 0.65gZn,有0.01 mol电子发生转移 |
| D、电池正极的反应为:Zn+2 OH--2e-=Zn(OH)2 |
| 0.65g |
| 65g/mol |


科目:高中化学 来源: 题型:
| A、10 g H2和10 g O2 |
| B、5.6 LN2(标准状况)和11 g CO2 |
| C、9 g H2O和11.2 L(标准状况)苯 |
| D、224 mL H2(标准状况)和0.1 mol N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C4H10和C20H42 |
| B、邻二甲苯和对二甲苯 |
| C、C4H8和C3H6 |
| D、一溴乙烷和1,2-二溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下4.48 L SO2和2.24 L O2充分反应后,生成0.2NASO3 |
| B、12 g SiO2原子晶体中含有0.4NASi-O键 |
| C、1.8 g冰中含有氢键数为0.4 NA |
| D、7.8 g Na2S和Na2O2混合物中含有的阴离子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、任何能使熵值增大的过程都能自发进行 |
| B、已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ?mol-1(Q>0),则将2 mol SO2(g) 和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| C、化学平衡发生移动,平衡常数一定发生变化 |
| D、足量的锌粒分别和等体积同浓度的 CH3COOH、HCl反应,两者放出氢气质量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
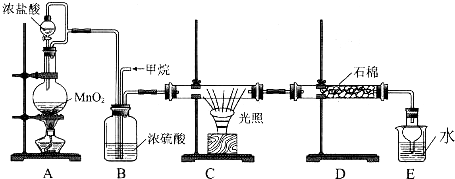
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com