
| A. | Na+、Cl-、OH- | B. | Na+、Cl-、OH-、AlO2- | ||
| C. | Na+、Cl-、Al3+ | D. | Na+、Cl-、AlO2-、Al3+ |
分析 2.3g钠的物质的量n=$\frac{m}{M}$=$\frac{2.3g}{23g/mol}$=0.1mol,2Na+2H2O=2NaOH+H2↑,根据钠原子守恒得n(Na)=n(NaOH)=0.1mol,n(AlCl3)=0.1mol/L×0.2L=0.02mol,NaOH和AlCl3反应方程式为3NaOH+AlCl3=Al(OH)3↓+3NaCl、4NaOH+AlCl3=NaAlO2+3NaCl,根据n(NaOH)、n(AlCl3)的关系确定产物成分.
解答 解:2.3g钠的物质的量n=$\frac{m}{M}$=$\frac{2.3g}{23g/mol}$=0.1mol,2Na+2H2O=2NaOH+H2↑,根据钠原子守恒得n(Na)=n(NaOH)=0.1mol,n(AlCl3)=0.1mol/L×0.2L=0.02mol,NaOH和AlCl3反应方程式为3NaOH+AlCl3=Al(OH)3↓+3NaCl、4NaOH+AlCl3=NaAlO2+3NaCl,
当n(NaOH):n(AlCl3)>4时生成NaAlO2;
当n(NaOH):n(AlCl3)<3时生成Al(OH)3;
当3<n(NaOH):n(AlCl3)<4时,生成Al(OH)3、NaAlO2,
实际上n(NaOH):n(AlCl3)=0.1mol:0.02mol=5>4,所以其产物为NaAlO2,
反应后溶液中存在Na+、Cl-、OH-、AlO2-,
故选B.
点评 本题考查了物质间反应,为高频考点,侧重于学生的分析能力的考查,明确氢氧化钠和氯化铝反应产物的分界点是解本题关键,再结合氢氧化钠和氯化铝物质的量的关系解答即可,题目难度不大.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:填空题
 用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),则CH3COOH的电离平衡常数Ka=2×10-5mol/L.
用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),则CH3COOH的电离平衡常数Ka=2×10-5mol/L.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将一根未打磨的铝条放入硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
| B | 将带火星的木条放入氧气瓶中 | 木条复燃 | 氧气能支持燃烧 |
| C | 将CO通过灼热的氧化铜 | 黑色固体变成红色 | CO具有可燃性 |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
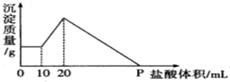 将由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水,充分反应后得到0.58g白色沉淀,向所得的浊液中逐滴加入0.5mol/L的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:
将由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水,充分反应后得到0.58g白色沉淀,向所得的浊液中逐滴加入0.5mol/L的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
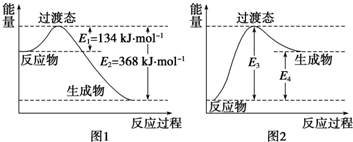
 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | a | b | c | d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,但不能直接与水反应生成H2SiO3 | |
| B. | N2是大气中的主要成分之一,雷雨时可直接转化为NO2 | |
| C. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com