
分析 氯化铝溶液中加入少量氢氧化钠溶液生成白色沉淀氢氧化铝,Al(OH)3具有两性,继续加入氢氧化钠溶液沉淀会溶解消失,以此解答该题.
解答 解:在AlCl3 溶液中滴加少量NaOH溶液,反应生成氢氧化铝白色沉淀,发生3NaOH+AlCl3=Al(OH)3↓+3NaCl,反应的离子方程式为:Al3++3OH-=Al(OH)3↓,继续加入氢氧化钠溶液,Al(OH)3具有两性,可与NaOH反应生成NaAlO2,发生Al(OH)3+NaOH=NaAlO2+2H2O,氢氧化铝沉淀消失,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:白色沉淀;Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查了铝的化合物性质、离子方程式书写,题目难度不大,明确铝及其化合物性质为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流 | |
| B. | 除去苯中的少量苯酚:加入适量NaOH溶液,振荡、静置、分液 | |
| C. | 检验甲酸中是否混有乙醛,可向样品中加入足量NaOH溶液以中和甲酸后,再做银镜反应实验或与新制Cu(OH)2共热的实验 | |
| D. | 液态溴乙烷中加入稀NaOH溶液共煮几分钟,然后加入足量稀硝酸,再加入AgNO3溶液检验溴乙烷中是否含有溴元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)2→Fe(OH)3 | B. | FeCl3→FeCl2 | C. | Al2O3→Al(OH)3 | D. | Na2CO3→NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若有白烟产生则管道漏气 | B. | 该反应中NH4Cl是还原产物 | ||
| C. | 反应中NH3只显还原性 | D. | 生成1.4g N2时转移0.3mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.5mol/L | B. | 18mol/L | C. | 3mol/L | D. | 9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4-、Cu2+、Cl-、NO3- | B. | K+、Na+、CO32-、SO4- | ||
| C. | K+、Mg2+、NO3-、SO4- | D. | Ba2+、NO3-、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24Cr的外围电子排布式:3d44s2 | B. | CO2的立体结构模型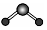 | ||
| C. | 基态碳原子的价电子排布图为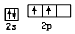 | D. | S2-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解度 MnS<PbS | |
| B. | MnS存在沉淀溶解平衡 MnS(s)?Mn2+(aq)+S2-(aq) | |
| C. | Cu2+转化为沉淀的原理为 MnS(s)+Cu2+(aq)═CuS(s)+Mn2+(aq) | |
| D. | 沉淀转化能用于除去溶液中的某些杂质离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com