
【题目】下列有关电池的说法不正确的是( )
A. 手机上用的锂离子电池属于二次电池
B. 锌锰干电池中,锌电极是负极
C. 氢氧燃料电池可把化学能转化为电能
D. 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
科目:高中化学 来源: 题型:
【题目】A1-MnO4电池是一种高能电池,以Ga2O3为缓蚀剂,其示意图如图所示。已知电池总反应为Al + MnO4 ═AlO2- + MnO2.下列说法正确的是( )

A. 电池工作时,K+向负极移动
B. 电池工作时,电子由Al经电解质溶液流向Ni
C. 负极反应为Al- 3e + 4OH ═AlO2 + 2H2O
D. 电池工作时,Ni电极周围溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组物质中含有的化学键类型相同的是( )
A. NaCl、HCl、H2O、NaOH B. HBr、CO2、H2O、CS2
C. Cl2、Na2S、HCl、SO2 D. Na2O2、H2O2、H2O、O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
① CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H=______kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H=______kJ·mol-1。
(2)反应①达平衡后采取下列措施,能提高CH3OH产率的有__________。
A.加入H2 B.升高温度 C.增大压强 D.使用催化剂
(3)在一定温度下,将4mol CO和4mol H2混合置于2L的密闭容器中发生反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),60s时达到平衡状态时,测得气体的总物质的量为4mol。达平衡时,氢气的转化率为__________,用CO表示的反应速率为__________,该反应的平衡常数为__________。
CH3OCH3(g)+CO2(g),60s时达到平衡状态时,测得气体的总物质的量为4mol。达平衡时,氢气的转化率为__________,用CO表示的反应速率为__________,该反应的平衡常数为__________。
(4)以下说法能说明反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)达到平衡状态的有__________。
CH3OCH3(g)+CO2(g)达到平衡状态的有__________。
A. 氢气和二氧化碳的浓度之比为3∶1
B.单位时间内断裂3个H-H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(5)二甲醚燃料电池的工作原理如图所示:
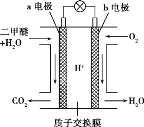
该电池负极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的说法不正确的是 ( )
A. 化石能源物质内部贮存着大量的能量
B. 植物的光合作用使太阳能转化为化学能
C. 燃料燃烧时只是将化学能转化为热能
D.由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池有广泛的用途。
Ⅰ.依据氧化还原反应:Cu+2Ag+===Cu2++2Ag设计的原电池如图所示。请回答下列问题:
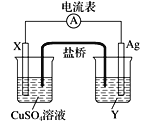
(1)电极X的材料是________________,电解质溶液Y是____________。
(2)银电极的电极反应式是______________________________。
(3)外电路中的电子是从_____极流向_____极。(填“正”或“负”)
(4)该原电池的正极是____________,还可以选用__________________等材料。
Ⅱ.铅蓄电池是化学电源,它工作时的电池总反应为:PbO2+Pb+2H2SO4===2PbSO4+2H2O。试回答:
(5)蓄电池负极的电极材料是_____________________(填“PbO2”或“Pb”)。
(6)工作时该蓄电池正极的电极反应式是___________。
(7)铅蓄电池工作时,电解质溶液的密度________(填“增大”、“减小”或“不变”),负极质量____ (填“增大”、“减小”或“不变”)。
Ⅲ.某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
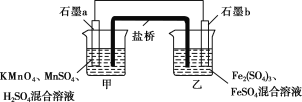
回答下列问题:
(8)此原电池的正极是石墨________(填“a”或“b”),发生________反应。
(9)电池工作时,盐桥中的SO![]() 移向________(填“甲”或“乙”)烧杯。
移向________(填“甲”或“乙”)烧杯。
(10)甲烧杯中的电极反应式为________________________________。
(11)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如图:根据要求填空:
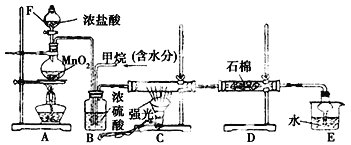
(1)实验室制取Cl2的化学方程式为:____________________。
(2)写出CH4与Cl2生成一氯代物的化学方程式____________________。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③________。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是________________________。
(5)E装置的作用是________。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(6)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法为__________。
(7)该装置还有缺陷,原因是没有进行尾气处理,尾气的主要成分是(双选,填编号)________。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国科学家日前利用卫星数据和一种先进的仪器,绘制了一幅地球上空二氧化氮的分布图。从科学家绘制的二氧化氮分布图看,欧洲和北美洲的一些经济比较发达,注重环保的大城市上空二氧化氮密度很高。其原因是这些地区的( )
A.硝酸工业发达
B.雷雨天气较多
C.机动车辆过多
D.燃料以煤为主
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H=?
2N2(g) +6H2O(g) △H=?
(1)
化学键 | H—O | O===O | N≡N | N—H |
键能kJ·molˉ1 | a | b | c | d |
△H=__________________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是__________________。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
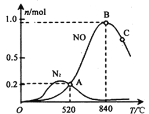
①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
②520℃时,4NH3(g)+5O2![]() 4NO(g) +6H2O(g)的平衡常数K=___________________ (不要求得出计算结果,只需列出数字计算式)。
4NO(g) +6H2O(g)的平衡常数K=___________________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
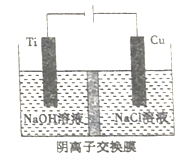
(4)纳米级Cu2O 由于具有优良的催化性能而受到关注,工业上常用电解法Cu2O,其反应为2Cu+H2O![]() Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为___________________,当生成_______克Cu2O时,就会有NA个阴离子通过离子交换膜。
Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为___________________,当生成_______克Cu2O时,就会有NA个阴离子通过离子交换膜。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com