
| A. | PH3比NH3稳定 | |
| B. | S2-半径比Cl-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na强 | |
| D. | 把钾放入氯化钠的水溶液中可制得金属钠 |
分析 A.元素的非金属性越强,对应的氢化物越稳定;
B.具有相同核外电子排布的离子,核电荷数越大离子半径越小;
C.同主族元素从上到下,金属性增强;
D.钾与水剧烈反应.
解答 解:A.非金属性N>P,元素的非金属性越强,对应的氢化物越稳定,故A错误;
B.S2-、Cl-具有相同核外电子排布,核电荷数越大离子半径越小,则S2-半径比Cl-的大,故B错误;
C.同主族元素从上到下,金属性增强,则Cs失电子能力比Na强,故C正确;
D.钾与水剧烈反应,不能置换出钠,故D错误.
故选C.
点评 本题考查元素周期率知识,为高考常见题型,侧重于元素周期表、周期率知识的综合理解和运用的考查,把握递变规律和比较角度,难度不大.


科目:高中化学 来源: 题型:解答题
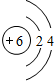 .
. ;写出C2B2的电子式
;写出C2B2的电子式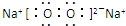 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 肼和氧气在相同催化剂和不同温度下生成的产物如图所示.已知在800℃下,容积固定的密闭容器中发生反应①、②:
肼和氧气在相同催化剂和不同温度下生成的产物如图所示.已知在800℃下,容积固定的密闭容器中发生反应①、②:| A. | v(N2)=v(NO) | |
| B. | 反应①的△H保持恒定 | |
| C. | 体系的密度不再发生变化 | |
| D. | 混合气体的平均相对分子质量不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H、C、O、K | B. | H、N、O | C. | H、O、S | D. | H、O、S、Na |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol乙烷中共价键总数为6NA | |
| B. | 1mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.1mol丙烯酸中含有双键的数目为0.2NA | |
| D. | 标准状况下,11.2L苯中含有分子的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Co(NH3)4 Cl2]Cl | B. | [Cu(NH3)4]Cl2 | C. | [Co(NH3)6]Cl3 | D. | [Co(NH3)3 Cl3] |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 除去甲苯中的苯甲酸,可以先加入NaOH溶液,充分振荡,然后分液 | |
| B. | 除去C2H5OH中的少量CH3COOH:加足量CaO,蒸馏 | |
| C. | 用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO | |
| D. | 除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸将乙酸全部转化为乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学电源名称 | 正极反应式 | 负极反应式 | 电解质溶液pH的变化 |
| 碱性氢氧燃料电池 | O2+2H2O+4e-=4OH- | 此空不用填写 | 变小 |
| 碱性甲烷燃料电池 | 此空不用填写 | CH4+8e-+10OH-=CO32-+7H2O | 变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态 | |
| B. | 用M表示此反应速率是0.1 amol•(L•min)-1 | |
| C. | 用X表示此反应的反应速率是(0.1-0.2 a)mol•(L•min)-1 | |
| D. | 当混合气体的压强不再发生变化时,说明反应达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com