
分析 (1)无水硝酸铜分解生成CuO时,生成的NO2与O2恰好与水完全反应,多余的气体为CuO分解生成的氧气,根据4CuO~O2计算剩余氧气的物质的量,再根据V=nVm计算体积;根据n=$\frac{m}{M}$计算5.64g无水硝酸铜物质的量,由转化关系可知,5.64g无水硝酸铜中含有的硝酸根等于溶液中含有的硝酸根,再根据c=$\frac{n}{V}$计算;
(2)残留固体可能是CuO和Cu2O的混合物,也可能是CuO和Cu(NO3)2的混合物,据此讨论结合铜原子守恒计算;
(3)根据固体质量减少与氧化铜中含有的氧元素质量,判断氧化铜是否完全发生转化为Cu,进而判断剩余固体中Cu元素、O元素的质量,确定Cu原子与氧原子关系,确定剩余固体的组成,据此计算解答;
(4)过滤得到ygCu来源于氢气还原生成的Cu及Cu2O与酸反应生成的Cu,令氢气还原生成的Cu的物质的量为nmol,则Cu2O的物质的量分别nxmol,根据方程式计算Cu2O与酸反应生成的Cu的物质的量,进而计算n的值,再根据Cu原子守恒计算为分解的Cu.
解答 解:(1)无水硝酸铜分解生成CuO时,生成的NO2与O2恰好与水完全反应,多余的气体为CuO分解生成的氧气,由可知关系式4CuO~O2可知,n(O2)=0.03mol×$\frac{1}{4}$=0.0075(mol),所以标准状况下氧气的体积为0.0075mol×22.4L/mol=0.168 L,
5.64g无水硝酸铜物质的量为$\frac{5.64g}{188g/mol}$=0.03mol,由转化关系可知,5.64g无水硝酸铜中含有的硝酸根等于溶液中含有的硝酸根,故溶液中硝酸根的物质的量为0.03mol×2=0.06mol,故稀释后溶液中硝酸根的物质的量浓度为$\frac{0.06mol}{0.1L}$=0.6mol/L,
故答案为:O2;0.168L;0.6mol/L;
(2)残留固体可能是CuO和Cu2O的混合物,也可能是CuO和Cu(NO3)2的混合物.若为CuO和Cu2O的混合物,则n(CuO)=$\frac{1.6g}{80g/mol}$=0.02 mol,n(CuO)+2n(Cu2O)=0.03 mol,所以n(Cu2O)=0.005 mol,故m(Cu2O)=144g/mol×0.005mol=0.72g,m(残留固体)=1.60 g+0.72 g=2.32 g; 若为CuO和Cu(NO3)2的混合物,则n(CuO)=0.02 mol,则n(CuO)+n[Cu(NO3)2]=0.03 mol,n[Cu(NO3)2]=0.01 mol,m[Cu(NO3)2]=0.01mol×188g/mol=1.88 g,m(残留固体)=1.60 g+1.88 g=3.48 g,故答案为:2.32g或3.48g;
(3)取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,则生成的氧气的质量为8g-6.88g=1.12g,8gCuO中O元素质量为8g×$\frac{16}{80}$=1.6g>1.12g,则CuO为完全转化为Cu,剩余固体中Cu元素质量为8g-1.6g=6.4g,O元素质量为1.6g-1.12g=0.28g,剩余固体中n(Cu):n(O)=$\frac{6.4}{64}$:$\frac{0.48}{16}$=10:3,故剩余固体为Cu、Cu2O,故n(Cu2O)=n(O)=$\frac{0.48g}{16g/mol}$=0.03mol,n(Cu)=$\frac{6.4g}{64g/mol}$-0.03mol×2=0.04mol,故n(Cu2O):n(Cu)=0.03mol:0.04mol=3:4,
故答案为:n(Cu2O):n(Cu)=3:4;
(4)8.00g CuO的物质的量为$\frac{8g}{80g/mol}$=0.1mol,
令氢气还原生成的Cu的物质的量为nmol,则Cu2O的物质的量分别nxmol,则:
Cu2O+2H+=Cu+Cu2++H2O
nx n
所以nx+n=$\frac{y}{64}$,故n=$\frac{y}{64(x+1)}$,故n(Cu2O)=nx=$\frac{xy}{64(x+1)}$,
根据铜原子守恒可知,未被还原的CuO的物质的量为n(CuO)=0.1-n-2nx=0.1-$\frac{y}{64(x+1)}$-2×$\frac{xy}{64(x+1)}$=0.1-$\frac{y+2xy}{64(x+1)}$,故答案为:n(CuO)=0.1-$\frac{y+2xy}{64(x+1)}$.
点评 本题考查混合物的有关计算、根据方程式的计算等,难度较大,注意(2)根据可能的情况进行讨论计算,对学生的思维由较高的要求.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | NaCl=Na++Cl- | B. | H2SO4=2H++SO42- | ||
| C. | Ca(OH)2=Ca2++2OH- | D. | Al2(SO4)3=Al3++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
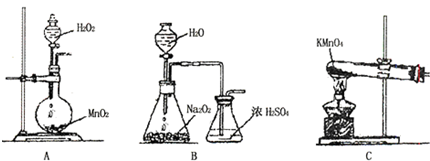
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子排布完全相同的两种微粒的化学性质一定相同 | |
| B. | 单原子形成的离子一定具有稀有气体元素原子的核外电子排布 | |
| C. | 核外电子排布相同的两种粒子一定属于同种元素 | |
| D. | 不存在质子数和电子数分别相同的阳离子和阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
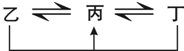 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系: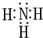 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
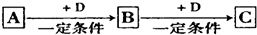
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | Cu | Fe | 盐酸 | 过滤 |
| B | AlCl3 | NaAlO2 | 盐酸 | - |
| C | FeCl2溶液 | FeCl3 | Fe | - |
| D | NaHCO3溶液 | Na2CO3 | CO2 | - |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅用新制氢氧化铜悬浊液(可以加热)不能通过化学方法完成对葡萄糖溶液、乙醇和乙酸溶液的鉴别 | |
| B. | 利用加碳酸钠饱和溶液和分液的方法可以除去乙酸乙酯中的乙酸和乙醇 | |
| C. | CH3CH2CH2OH和CH3CH2CH2Cl的同分异构体数目相同 | |
| D. | 石油的分馏、裂化,煤的干馏,都是通过化学变化获得新物质的工业生产方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com