
阿伏加德罗常数用NA表示,下列叙述正确的是
①标准状况下,22.4L乙醇中含有的氧原子数目为NA
②1L1 mol·L-1NH4Cl溶液中NH4+数目为NA
③0.44gC3H8中含有的共价键总数目为0.1NA
④25℃时,1LpH=13的Ba(OH)2溶液中含有OH-数目为0.2NA
⑤6.4g的S2和S8混合物中,含硫原子总数为0.2NA
⑥11.2LCl2通入足量氢氧化钠溶液中充分反应,转移的电子数等于0.5NA
A.③⑤ B.②⑤ C.③④ D.⑤⑥
A
【解析】
试题分析:①在标准状况下,乙醇是液体,不能使用气体摩尔体积,错误;②在溶液中NH4+会发生水解反应而消耗,使用1L1 mol·L-1NH4Cl溶液中NH4+数目小于NA,错误;③0.44gC3H8的物质的量是0.01mol,其中含有的共价键总数目为0.01×10NA=0.1NA,正确;④25℃时,1LpH=13的Ba(OH)2溶液中含有OH-数目为0.1NA,错误;⑤由于S原子的相对原子质量是32,使用6.4g的S2和S8混合物中,含硫原子总数为0.2NA,正确;⑥11.2LCl2由于缺少条件,使用其物质的量不一定是0.5mol,因此通入足量氢氧化钠溶液中充分反应,转移的电子数不一定等于0.5NA,错误。
考点:考查阿伏加德罗常数的有关计算的知识。


科目:高中化学 来源:2015届广东省中山市等五校联考高三第一学期化学试卷(解析版) 题型:选择题
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应,二者相比较,相等的是
A.铜片完全消耗时所用的时间
B.反应中转移的电子总数
C.反应所消耗硝酸的物质的量
D.反应生成气体的体积(标准状况)
查看答案和解析>>
科目:高中化学 来源:2015届山西省高三上学期期中考试化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子反应方程式为
A.大理石溶于醋酸溶液: CaCO3 + 2H+==Ca2+ + CO2 ↑+ H2O
B.向FeBr2溶液中通入足量氯气:2Fe2+ + 4Br- + 3Cl2=== 2Fe3+ + 2Br2 + 6Cl-
C.NH4HCO3溶于过量的NaOH溶液中: HCO3- + OH- === CO32- + H2O
D.向明矾(KAl(SO4)2·12H2O)溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3+ + 3SO42- + 3Ba2+ + 6OH-=== 2Al(OH)3↓ + 3BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次月考联考化学试卷(解析版) 题型:选择题
在1 L含0.1 mol Na[Al(OH)4] 和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol·L-1的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是
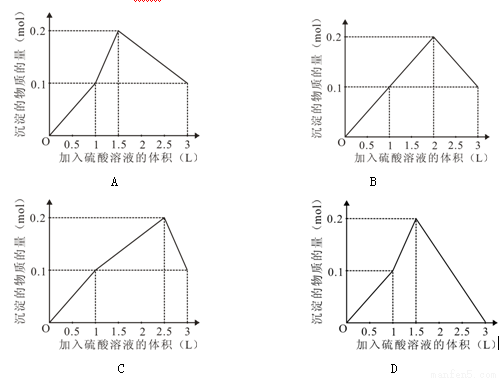
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次月考联考化学试卷(解析版) 题型:选择题
下列各组离子在溶液中能够大量共存,且加入金属铝后只有氢气放出的是
A.H+、Al3+、Cl‑、SO32- B.Na+、K+、OH‑、[Al(OH)4]-
C.H+、K+、SO42-、NO3‑ D.Na+、NH4+、Cl-、OH‑
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次月考联考化学试卷(解析版) 题型:选择题
下列推断正确的是
A.SiO2 是酸性氧化物,能与NaOH溶液反应
B.Na2O、Na2O2组成元素相同,与 CO2反应产物也相同
C.CO、NO、 NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
查看答案和解析>>
科目:高中化学 来源:2015届山东省邹城市高三10月月考化学试卷(解析版) 题型:填空题
(14分)某实验小组配制0.10mol/L NaOH溶液并进行有关性质实验,回答下列问题。
(1)若实验中大约要使用475mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母) 。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 | | | | | | |
序号 | A | B | C | D | E | F |
(3)下列情况会使所配溶液浓度偏低的是(填序号)
①称量时,左盘高,右盘低
②固体溶解后未冷却到室温就直接转移到容量瓶中
③溶液转移到容量瓶后,未进行洗涤操作
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度实验室欲配制
(4)向VmL上述浓度的NaOH溶液中,通入一定量的CO2后,然后向该溶液中逐滴加入1mol L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如下图所示:
L-1的盐酸,所加入盐酸溶液的体积与产生CO2的体积关系如下图所示:
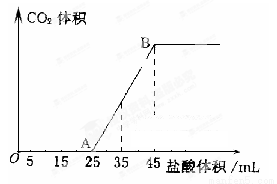
①当加入35.0mL盐酸溶液时,产生标准状况下二氧化碳的体积为__________mL;
②计算所取氢氧化钠溶液的体积V=__________mL。
(5)取上述氢氧化钠溶液200mL,加入适量铝粉使之恰好完全反应,该反应的化学方程式为__________________________________,逐渐向反应后的溶液中至少加入1.0 mol L-1的盐酸________ mL才能使生成的沉淀完全溶解。
L-1的盐酸________ mL才能使生成的沉淀完全溶解。
查看答案和解析>>
科目:高中化学 来源:2015届山东省菏泽市高三上学期期中联考化学试卷(A)(解析版) 题型:实验题
(13分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
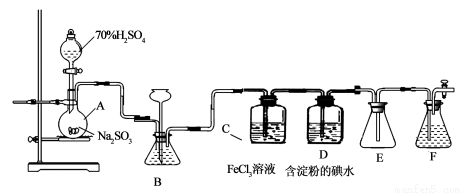
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若
,则整个装置气密性良好。装置E的作用是 。装置F中为 溶液。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
A.蒸馏水 B.饱和Na2SO3溶液
C.饱和NaHSO3溶液 D.饱和NaHCO3溶液
(3)SO2气体还原Fe3+反应的产物是________________(填离子符号)。
(4)在上述装置中通入过量的SO2为了验证C中SO2与Fe3+发生了氧化还原反应,他们取C中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是____,原因是_______________________________________。
(5)能表明I-的还原性弱于SO2的现象是_________________,写出有关离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列对化学知识概括合理的是( )
A.酸性氧化物都是非金属氧化物
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
D.熔融状态能导电的物质一定是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com