
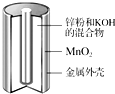
 碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.
碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.分析 (1)原电池中Zn转化为Zn(OH)2,Zn化合价升高,失电子,做负极,正极上发生得电子的还原反应;
(2)金属锌和氢氧化钾之间反应生成偏锌酸钾和氢气;
(3)利用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极.阳极与电池的正极相连发生氧化反应,依次是Zn、Fe、Cu放电,阴极与电池的负极相连发生还原反应Cu2++2e-═Cu,根据电极反应结合电子守恒进行计算.
解答 解:(1)原电池中Zn转化为Zn(OH)2,Zn化合价升高,失电子,做负极,正极上发生得电子的还原反应,电极反应式为:MnO2+H2O+e-═MnOOH+OH-,故答案为:Zn;MnO2+H2O+e-=MnOOH+OH-;
(2)金属锌和氢氧化钾之间反应生成偏锌酸钾和氢气,即Zn+2KOH=K2ZnO2+H2↑,故答案为:Zn+2KOH=K2ZnO2+H2↑;
(3)①利用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极,粗铜连接电源的正极,阳极与电池的正极相连发生氧化反应,依次是Zn、Fe、Cu放电,阴极与电池的负极相连发生还原反应:Cu2++2e-═Cu,电解一段时间后,CuSO4溶液的浓度减小,故答案为:正;减小;
②若阴极质量增重32g即0.5mol,根据电极反应:Cu2++2e-═Cu,转移电子是1mol,电池的正极反应:MnO2+H2O+e-═MnOOH+OH-,此时消耗MnO2的物质的量是:1mol,质量是87g,故答案为:87.
点评 本题考查学生原电池的工作原理以及应用知识,注意知识的迁移应用是关键,难度中等.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | X能形成化学式为H2XO4的酸 | |
| B. | X能与某些金属元素形成化合物 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X可能形成化学式为KXO3的盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同温同压下,相同体积的氟气和氩气所含的原子数相等 | |
| B. | 标准状况下,1.12 L NO与1.12 L O2的混合物中含有的原子数为0.2NA | |
| C. | 常温下,1L 0.1 mol•L-1 CuSO4溶液中含有的Cu2+数目为0.1NA | |
| D. | 25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
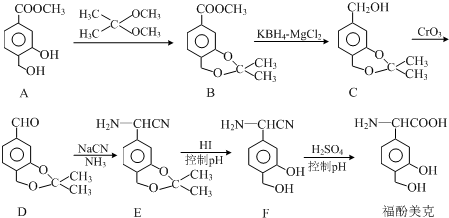
 .
.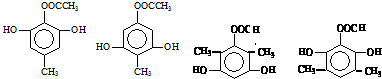 任意一种.
任意一种.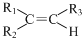 $→_{②Zn/H_{20}}^{①O_{3}}$
$→_{②Zn/H_{20}}^{①O_{3}}$ 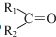 +R3CHO,根据已有知识并结合相关信息,写出以
+R3CHO,根据已有知识并结合相关信息,写出以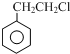 为原料制备
为原料制备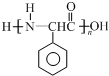 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.
;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式6Li+N2=2Li3N.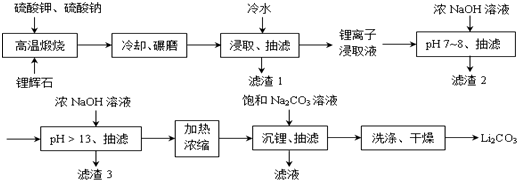
| 金属离子 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 沉淀完全的pH | 4.7 | 9.0 | 3.2 | 10.1 |
| 温度 溶解度 | 10℃ | 20℃ | 50℃ | 80℃ |
| Li2SO4 | 35.4 | 34.7 | 33.1 | 31.7 |
| Li2CO3 | 1.43 | 1.33 | 1.08 | 0.85 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含氧酸酸性R>X | B. | 简单氢化物稳定性Y<X | ||
| C. | 最高正化合价Z<X<Y<R | D. | 由Z和R形成的化合物为离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com